题目内容
9.(1)现有下列物质 a.铝 b.CO2 c.H2SO4 d.NaOH固体 e.氨水 f.NaHCO3晶体①上述各物质属于电解质的是(填序号,下同)cdf,能导电的是ae
②f在水中的电离方程式为NaHCO3=Na++HCO3-.
③足量的b通入d的溶液中反应的离子方程式为CO2+OH-=HCO3-
(2)焊接铜器时,可先用NH4Cl 除去其表面的氧化铜再进行焊接,该反应可表示为:
4CuO+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$3Cu+CuCl2+N2↑+4H2O
①用双线桥标明电子转移的方向和数目.
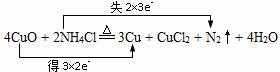 .
.②该反应中,还原剂与还原产物的物质的量之比为2:3.
③反应中若产生0.2mol的氮气,则有1.2mol的电子转移.
分析 (1)①在水溶液里或熔融状态下能导电的化合物是电解质,含有自由移动电子或离子的物质能导电;
②碳酸氢钠是强碱弱酸酸式盐,为强电解质,在水溶液中完全电离生成钠离子和碳酸氢根离子;
③足量二氧化碳和NaOH溶液反应生成碳酸氢钠;
(2)①该反应中部分Cu元素化合价由+2价变为0价、N元素化合价由-3价变为0价,所以生成Cu单质的Cu元素得电子、N元素失电子,转移电子数为6;
②失电子化合价升高的反应物是还原剂,得电子化合价降低的反应物是氧化剂,氧化剂对应的产物是还原产物,所以还原剂是氯化铵、还原产物是Cu,其系数之比等于物质的量之比;
③根据氮气和转移电子之间关系式计算.
解答 解:(1)①在水溶液里或熔融状态下能导电的化合物是电解质,含有自由移动电子或离子的物质能导电,这几种物质中属于电解质的是cdf,能导电的是ae,
故答案为:cdf;ae;
②碳酸氢钠是强碱弱酸酸式盐,为强电解质,在水溶液中完全电离生成钠离子和碳酸氢根离子,其电离方程式为NaHCO3=Na++HCO3-,故答案为:NaHCO3=Na++HCO3-;
③足量二氧化碳和NaOH溶液反应生成碳酸氢钠,离子方程式为CO2+OH-=HCO3-,故答案为:CO2+OH-=HCO3-;
(2)①该反应中部分Cu元素化合价由+2价变为0价、N元素化合价由-3价变为0价,所以生成Cu单质的Cu元素得电子、N元素失电子,转移电子数为6,电子转移方向和数目为 ,故答案为:
,故答案为: ;
;
②失电子化合价升高的反应物是还原剂,得电子化合价降低的反应物是氧化剂,氧化剂对应的产物是还原产物,所以还原剂是氯化铵、还原产物是Cu,其系数之比等于物质的量之比,所以还原剂和还原产物的物质的量之比为2:3,故答案为:2:3;
③根据氮气和转移电子之间关系得转移电子物质的量=0.2mol×2×[0-(-3)]=1.2mol,故答案为:1.2.
点评 本题考查氧化还原反应,涉及氧化还原反应计算、基本概念、化学用语等知识点,明确基本原理、基本概念是解本题关键,注意物质导电性与电解质的关系,导电的物质不一定是电解质,但电解质不一定导电,为易错点.

 天天向上口算本系列答案
天天向上口算本系列答案| A. | 滴加酚酞显无色溶液 | B. | 含有较多H+的溶液 | ||
| C. | pH<7的溶液 | D. | c(OH-)<c(H+)的溶液 |
| A. | 7.5 mL | B. | 17.5 mL | C. | 25.0 mL | D. | 35.0 mL |
| A. | 使无色酚酞试液呈红色的溶液中:Na+、K+、SO42-、CO32- | |
| B. | 无色透明的溶液中:Cu2+、K+、SO42-、NO3- | |
| C. | 含有大量BaCl2的溶液中:Mg2+、NH4+、SO42-、NO3- | |
| D. | 使紫色石蕊试液呈红色的溶液中:Na+、K+、CO32-、NO3- |
| A. | 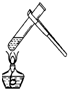 给试管加热 | B. | 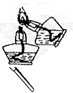 点燃酒精灯 | C. |  滴加液体 | D. | 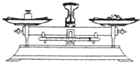 称量10.05g固体 称量10.05g固体 |
| A. | CH4 | B. | C2H4 | C. | C2H2 | D. | NH3 |
| A. | 1-己炔、甲苯、十一烷 | B. | 乙醇、苯、溴苯 | ||
| C. | 乙二醇、乙醛、硝基苯 | D. | 溴苯、四氯化碳、乙酸钠 |
| A. | 打开盛浓盐酸的试剂瓶可看到白色的酸雾,这说明HCl不稳定 | |
| B. | 蔗糖中滴入浓硫酸,蔗糖变黑,这说明浓硫酸具有脱水性 | |
| C. | FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| D. | 金属钠存放于煤油中 |