题目内容
在25°C时,0.1mol/L氯化铵溶液由水电离出来的[H+]=1×10-5mol/L,则该温度下此溶液中氨水的电离平衡常数Kb为多少?.
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:写出氨水电离方程式,计算出离子浓度,代入电离平衡常数表达式计算氨水的电离平衡常数.
解答:
解:NH4+在溶液中能发生水解反应,NH4++H2O?NH3?H2O+H+
故c(NH3?H2O)=c(H+)=1×10-5mol/L,则c(OH-)=
=
=10-9mol/L,c(NH4+)=0.1mol/L-1×10-5mol/L≈0.1mol/L,
氨水的电离方程式为:NH3?H2O?NH4++OH-
电离平衡常数Kb(NH3?H2O)=
,
把以上数据代入平衡常数表达式:Kb(NH3?H2O)=
=1×10-5mol/L,
答:该温度下此溶液中氨水的电离平衡常数Kb为1×10-5mol/L.
故c(NH3?H2O)=c(H+)=1×10-5mol/L,则c(OH-)=
| KW |
| c(H+) |
| 10-14 |
| 10-5 |
氨水的电离方程式为:NH3?H2O?NH4++OH-
电离平衡常数Kb(NH3?H2O)=
| [NH4+]?[OH-] |
| [NH3?H2O] |
把以上数据代入平衡常数表达式:Kb(NH3?H2O)=
| 0.1mol/L×10-9mol/L |
| 10-5mol/L |
答:该温度下此溶液中氨水的电离平衡常数Kb为1×10-5mol/L.
点评:本题考查了电离平衡常数的计算,难度较大,应根据电离平衡表达式,计算出相应离子浓度代入表达式即可.掌握基础是关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列日常生活中的现象与氧化还原反应无关的是( )
| A、铜铸塑像上出现铜绿[Cu2(OH)2CO3] |
| B、用石膏点豆腐 |
| C、不良商贩用硫黄熏蒸银耳制作“雪耳” |
| D、自来水厂用二氧化氯对水进行消毒 |
下列反应的离子方程式书写正确的是( )
| A、澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2═CaCO3↓+H2O |
| B、四氧化三铁溶于稀硝酸:Fe3O4+8H+=4H2O+Fe2++2Fe3+ |
| C、二氧化硅与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |
| D、硅酸与烧碱溶液中和:H2SiO3+2OH-═SiO32-+2H2O |
食品添加剂让食品变得丰富多彩,但应正确使用食品添加剂.做馒头的过程中不能添加的是( )
| A、增白剂 | B、蔗糖 |
| C、小苏打 | D、食盐 |


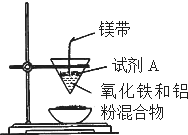 某小组进行铝热反应实验,装置如图所示.
某小组进行铝热反应实验,装置如图所示.