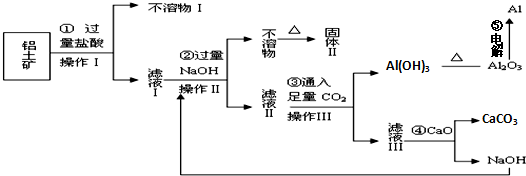
题目内容
下列解释事实的方程式不正确的是( )
| A、测0.1 mol/L氨水的pH为11:NH3?H2O?NH4++OH- | ||||
B、用CuCl2溶液做导电实验,灯泡发光:CuCl2
| ||||
| C、酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+?2Mn2++5O2↑+8H2O | ||||
| D、铅酸蓄电池的正极在充电时的反应:PbSO4+2H2O-2e-?PbO2+4H++SO42- |
考点:离子方程式的书写
专题:
分析:A.一水合氨电离为可逆反应;
B.溶液做导电实验,发生电解反应;
C.发生氧化还原反应,电子、电荷守恒;
D.正极在充电时,正极上硫酸铅失去电子,发生氧化反应.
B.溶液做导电实验,发生电解反应;
C.发生氧化还原反应,电子、电荷守恒;
D.正极在充电时,正极上硫酸铅失去电子,发生氧化反应.
解答:
解:A.测0.1 mol/L氨水的pH为11,发生电离的离子反应为NH3?H2O?NH4++OH-,故A正确;
B.CuCl2溶液做导电实验,首先电离CuCl2=Cu2++2Cl-,通电时发生电解:CuCl2
Cu+Cl2↑,故B错误;
C.酸性介质中KMnO4氧化H2O2的离子反应为2MnO4-+5H2O2+6H+?2Mn2++5O2↑+8H2O,故C正确;
D.铅酸蓄电池的正极在充电时的反应,阳极反应式为PbSO4+2H2O-2e-?PbO2+4H++SO42-,故D正确;
故选B.
B.CuCl2溶液做导电实验,首先电离CuCl2=Cu2++2Cl-,通电时发生电解:CuCl2
| ||
C.酸性介质中KMnO4氧化H2O2的离子反应为2MnO4-+5H2O2+6H+?2Mn2++5O2↑+8H2O,故C正确;
D.铅酸蓄电池的正极在充电时的反应,阳极反应式为PbSO4+2H2O-2e-?PbO2+4H++SO42-,故D正确;
故选B.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重电离、电解及电极反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
下列有关化学用语使用正确的是( )
A、HClO的电子式: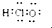 | ||
B、Mg2+的结构示意图: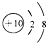 | ||
| C、乙酸乙酯的结构简式:CH3COOCCH3 | ||
D、具有16个质子,16个中子和18个电子的单核离子是
|
等质量的O2和O3中( )
| A、所含原子数相同 |
| B、所含分子数相同 |
| C、同温同压下,气体体积相同 |
| D、同温同压下,气体的密度相同 |
某元素的一个原子的质量为ag,一个12C原子的质量为bg,阿伏加德罗常数为NA,则该原子的相对原子质量数值可表示为( )
A、12
| ||
B、12
| ||
C、
| ||
| D、bNA |
下列物质中,所含分子数最多的是(NA表示阿伏加德罗常数)( )
| A、10 g H2 |
| B、2 mol Cl2 |
| C、1.5 NA CO2 |
| D、22.4 L O2(标准状况) |
下列离子方程式错误的是( )
| A、向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| B、Cl2通入NaOH溶液:Cl2+2OH-=Cl-+ClO-+H2O |
| C、AlCl3溶液中加入过量稀氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| D、将Na投入水中:2Na+2H2O=2Na++2OH-+H2↑ |
下列反应中不属于基本反应类型的是( )
| A、Cl2+H2O═HCl+HClO |
| B、Zn+H2SO4═ZnSO4+H2↑ |
| C、Na2O+H2O═2NaOH |
| D、NaCl+AgNO3═AgCl↓+NaNO3 |