题目内容
某芳香族酯类化合物甲的分子式为C14H10O5,1mol甲水解后只生成一种产物乙,其物质的量为2mol.下列说法不正确的是( )
| A、符合上述条件的甲共有3种 |
| B、1mol甲最多可以和4molNaOH反应 |
| C、乙能和浓溴水发生反应 |
| D、1mol乙最多消耗2molNaHCO3反应 |
考点:有机物的结构和性质,有机物结构式的确定
专题:
分析:酯类化合物甲含-COOC-,甲的分子式为C14H10O5,1mol甲水解后只生成一种产物乙,其物质的量为2mol,则乙中含-OH和-COOH,由碳原子数的关系可知,乙为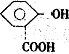 或
或 或
或 ,然后结合有机物的结构与性质来解答.
,然后结合有机物的结构与性质来解答.
 或
或 或
或 ,然后结合有机物的结构与性质来解答.
,然后结合有机物的结构与性质来解答.解答:
解:酯类化合物甲含-COOC-,甲的分子式为C14H10O5,1mol甲水解后只生成一种产物乙,其物质的量为2mol,则乙中含-OH和-COOH,由碳原子数的关系可知,乙为 或
或 或
或 ,
,
A.乙有3种,则发生酯化反应生成的甲有3种,故A正确;
B.甲中含酚-OH、-COOH、-COOC-,且水解生成的-COOH、-OH均与NaOH反应,则1mol甲最多可以和4molNaOH反应,故B正确;
C.乙中含酚-OH,能与溴水发生取代反应,故C正确;
D.酚-OH不能与NaHCO3反应,只有-COO均能与NaHCO3反应,则1mol乙最多消耗1molNaHCO3,故D错误;
故选D.
 或
或 或
或 ,
,A.乙有3种,则发生酯化反应生成的甲有3种,故A正确;
B.甲中含酚-OH、-COOH、-COOC-,且水解生成的-COOH、-OH均与NaOH反应,则1mol甲最多可以和4molNaOH反应,故B正确;
C.乙中含酚-OH,能与溴水发生取代反应,故C正确;
D.酚-OH不能与NaHCO3反应,只有-COO均能与NaHCO3反应,则1mol乙最多消耗1molNaHCO3,故D错误;
故选D.
点评:本题考查有机物的推断,明确酯化反应的规律及甲水解生成2mol乙可推出乙为解答本题的突破口,熟悉酚、羧酸、酯的性质即可解答,题目难度中等.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
自来水可以用氯气消毒、某学生用这种自来水去配制下列物质的溶液,不会产生明显的药品变质问题的是( )
①AgNO3 ②FeCl3 ③AlCl3 ④NaOH ⑤FeCl2 ⑥Na2CO3.
①AgNO3 ②FeCl3 ③AlCl3 ④NaOH ⑤FeCl2 ⑥Na2CO3.
| A、①②⑥ | B、③④ |
| C、②③ | D、④⑤⑥ |
稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易被氧化变暗,且受热易燃烧,遇水很快反应.下列说法正确的是(已知:铈常见的化合价有+3和+4,氧化性:Ce4+>Fe3+)( )
| A、电解熔融CeO2制Ce时,铈在阳极获得 | ||||||||
| B、铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑ | ||||||||
| C、用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+ | ||||||||
D、Ce有四种稳定的核素Ce
|
 已知:①C(s、金刚石)+O2(g)═CO2(g)△H1=-395.4kJ?mol-1
已知:①C(s、金刚石)+O2(g)═CO2(g)△H1=-395.4kJ?mol-1②C(s、石墨)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1,上述反应中的能量变化如图所示,下列说法正确的是( )
| A、石墨和金刚石之间的转化是物理变化 |
| B、C(s、金刚石)═C(s、石墨)△H=+1.9 kJ?mol-1 |
| C、金刚石比石墨的热稳定性好 |
| D、图中b代表反应①的能量变化 |
 得重感冒之后,常吃一种抗生素--头孢氨苄,分子式为C16H17N3O4S?H2O,其化学结构式如图,有关其说法正确的是( )
得重感冒之后,常吃一种抗生素--头孢氨苄,分子式为C16H17N3O4S?H2O,其化学结构式如图,有关其说法正确的是( )| A、在一定条件下,能发生水解反应生成氨基酸 |
| B、1mol该分子最多能与7molH2反应 |
| C、该分子能与碳酸钠反应,不能与盐酸反应 |
| D、头孢氨苄极易溶于水,能使溴水褪色 |
 按如图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )
按如图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )①c(Ag+) ②c(AgNO3) ③a棒的质量 ④b棒的质量 ⑤溶液的pH.
| A、①③ | B、③④ |
| C、①②⑤ | D、①②④ |
下列说法正确的是( )
| A、水是一种非常稳定的化合物,这是由于氢键所致 |
| B、乙醇分子中有一个手性碳原子 |
| C、离子晶体的晶格能越大离子键越强 |
| D、电负性Na>Al |