题目内容
下列电离方程式中,书写错误的是
- A.Ba(OH)2=Ba2++2 OH-
- B.H3PO4?3 H++PO43
- C.HClO?H++ClO-
- D.NH3?H2O?NH4++OH-
B
分析:A、氢氧化钡是强电解质,完全电离;
B、磷酸是弱电解质,部分电离,电离方程式分分步写;
C、次氯酸是弱电解质,部分电离,电离方程式用可逆号;
D、氨水是弱碱,部分电离,用可逆号连接.
解答:A、由于氢氧化钡是强电解质,溶液中完全电离,电离方程式是:Ba(OH)2═Ba2++2OH-,故A错误;
B、磷酸是弱电解质,不能完全电离,正确的电离方程式是:H3PO4?H++H2PO4-,故B正确;
C、次氯酸是弱酸,不能完全电离,电离方程式是:HClO?H++ClO-,故C错误;
D、氨水是弱电解质,溶液中部分电离,电离方程式为:NH3?H2O?NH4++OH-,故D错误;
故选B.
点评:本题考查电离方程式的书写,多元的弱电解质电离要分步写,弱电解质存在电离平衡,本题难度较低,注重了基础知识考查.
分析:A、氢氧化钡是强电解质,完全电离;
B、磷酸是弱电解质,部分电离,电离方程式分分步写;
C、次氯酸是弱电解质,部分电离,电离方程式用可逆号;
D、氨水是弱碱,部分电离,用可逆号连接.
解答:A、由于氢氧化钡是强电解质,溶液中完全电离,电离方程式是:Ba(OH)2═Ba2++2OH-,故A错误;
B、磷酸是弱电解质,不能完全电离,正确的电离方程式是:H3PO4?H++H2PO4-,故B正确;
C、次氯酸是弱酸,不能完全电离,电离方程式是:HClO?H++ClO-,故C错误;
D、氨水是弱电解质,溶液中部分电离,电离方程式为:NH3?H2O?NH4++OH-,故D错误;
故选B.
点评:本题考查电离方程式的书写,多元的弱电解质电离要分步写,弱电解质存在电离平衡,本题难度较低,注重了基础知识考查.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
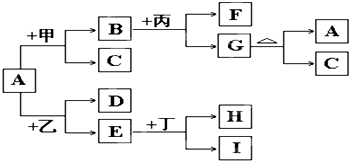
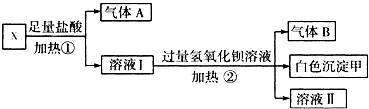
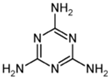 近期,质检部门在众多品牌乳制品中检出有毒有机物三聚氰胺[C3N3(NH2)3],其分子结构如图所示.在乳制品行业掀起了一场轩然大波,引发了一场关于食品安全问题的大讨论.三聚氰胺是一种重要的有机化工原料,因其含氮量高而被不法商家用作食品添加剂,以提升食品检测中的蛋白质含量指标,因此三聚氰胺也被人称为“蛋白精”.三聚氰胺遇强酸或强碱水溶液水解,氨基逐步被羟基取代,最后生成三聚氰酸[C3N3(OH)3].三聚氰酸可用于消除汽车尾气中的NO2,其反应原理为:C3N3(OH)3=3HNCO;8HNCO+6NO2=7N2+8CO2+4H2O.下列说法正确的是
近期,质检部门在众多品牌乳制品中检出有毒有机物三聚氰胺[C3N3(NH2)3],其分子结构如图所示.在乳制品行业掀起了一场轩然大波,引发了一场关于食品安全问题的大讨论.三聚氰胺是一种重要的有机化工原料,因其含氮量高而被不法商家用作食品添加剂,以提升食品检测中的蛋白质含量指标,因此三聚氰胺也被人称为“蛋白精”.三聚氰胺遇强酸或强碱水溶液水解,氨基逐步被羟基取代,最后生成三聚氰酸[C3N3(OH)3].三聚氰酸可用于消除汽车尾气中的NO2,其反应原理为:C3N3(OH)3=3HNCO;8HNCO+6NO2=7N2+8CO2+4H2O.下列说法正确的是