题目内容
10.下列各组离子在溶液中能大量共存,加入OH-有沉淀析出,加入H+能放出气体的是( )| A. | Na+、C1-、NO3-、H+ | B. | K+、Cl-、SO42-、H | ||
| C. | Fe3+、C1-、SO42-、NH4+ | D. | Ca2+、HCO3-、Cl-、NO3- |
分析 根据离子之间不能结合生成沉淀、气体、水等,则离子大量共存,并结合加入OH-有沉淀析出,加入H+能放出气体来解答.
解答 解:A.该组离子之间不反应,可大量共存,但加入H+或OH-均无明显现象,故A不选;
B.该组离子之间不反应,可大量共存,但加入H+或OH-均无明显现象,故B不选;
C.该组离子之间不反应,可大量共存,加入OH-会有Fe(OH)3沉淀,加入H+无现象,故C不选;
D.该组离子之间不反应,可大量共存,加入OH-,HCO3-+OH-+Ca2+=CaCO3↓+H2O;加入H+,H++HCO3-=H2O+CO2↑,故D选;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
20.下列有关说法正确的是( )
| A. | 常温下,pH=8的碱性溶液中不可能存在H2CO3分子 | |
| B. | 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 | |
| C. | 0.1mol/LCH3COOH溶液加水稀释,溶液的pH和CH3COOH的电离度均增大 | |
| D. | 将BaCl2溶液滴入含酚酞的Na2CO3溶液,红色褪去,说明BaCl2溶液显酸性 |
1.维生素C的结构简式如图,有关它的叙述错误的是( )
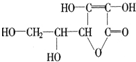

| A. | 是一个环状的酯类化合物 | B. | 易起加成及氧化反应 | ||
| C. | 可以溶解于水 | D. | 在碱性溶液中能稳定地存在 |
5.已知A、B、D、E 均为中学化学常见物质,它们之间的转化关系如图所示(部分产物略去,①②③④的反应条件相同).则A、E 可能的组合为( )
①CO2、NaOH 溶液 ②NaCl溶液、Ca(OH)2 溶液③Fe、稀HNO3 ④Na、O2 ⑤CuO、C ⑥AlCl3 溶液、NH3•H2O.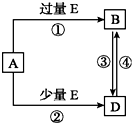
①CO2、NaOH 溶液 ②NaCl溶液、Ca(OH)2 溶液③Fe、稀HNO3 ④Na、O2 ⑤CuO、C ⑥AlCl3 溶液、NH3•H2O.

| A. | ②③④⑤ | B. | ①③④⑤⑥ | C. | ①②③⑤⑥ | D. | ①③⑤ |
15.欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO${\;}_{3}^{2-}$)、c(HCO3?)都减少,其方法是( )
| A. | 加入氢氧化钠固体 | B. | 加水 | ||
| C. | 通入二氧化碳气体 | D. | 加入饱和石灰水溶液 |
20.某溶液中可能含有下列5种离子中的某几种:Na+、NH4+、Fe3+、Al3+、Clˉ.为确认该溶液组成进行如下实验:
①取20.0mL该溶液,加入20.0mL 4.00mol•L-1NaOH溶液,生成红褐色沉淀且没有刺激性气体生成.将沉淀过滤、洗涤、灼烧,得固体0.80g.再将滤液稀释至100mL,测得滤液中c(OHˉ)为0.10mol•L-1;
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀8.61g.
由此可得出原溶液组成的正确结论是( )
①取20.0mL该溶液,加入20.0mL 4.00mol•L-1NaOH溶液,生成红褐色沉淀且没有刺激性气体生成.将沉淀过滤、洗涤、灼烧,得固体0.80g.再将滤液稀释至100mL,测得滤液中c(OHˉ)为0.10mol•L-1;
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀8.61g.
由此可得出原溶液组成的正确结论是( )
| A. | 一定含有Fe3+、Al3+、Clˉ,不含Na+、NH4+ | |
| B. | 一定含有Na+、Fe3+、Clˉ,不含NH4+,可能含有Al3+ | |
| C. | c (Al3+)=1.00 mol•L-1 | |
| D. | c(Na+)=0.50 mol•L-1 |
 某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:
某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置: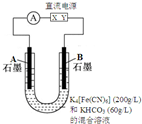 气态废弃物中的硫化氢可用下法转化为可利用的硫.
气态废弃物中的硫化氢可用下法转化为可利用的硫.