题目内容
14.用H2还原mgCuO,当大部分固体变红时停止加热,冷却后称得残留固体质量为ng.则被还原的CuO的质量为( )| A. | 40Wg | B. | 80ng | C. | 5(m-n)g | D. | mg |
分析 发生反应:H2+CuO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,反应前后固体质量差为氧化铜在反应中失去氧元素的质量,结合CuO中氧元素质量分数计算CuO的质量.
解答 解:发生反应:H2+CuO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,反应前后固体质量差为氧化铜在反应中失去氧元素的质量,故反应中氧化铜失去O元素的质量=mg-ng=(m-n)g,故被还原的CuO的质量=(m-n)g÷$\frac{16}{80}$=5(m-n)g,
故选C.
点评 本题考查化学方程式的有关计算,明确固体质量变化是解题关键,侧重考查学生的分析思维能力,注意判断消耗氢气实际质量,学生容易忽略“为防止生成的铜被氧化,要继续通入氢气直至冷却”,难度中等.

练习册系列答案
相关题目
5.下列各组物质中,分子数相同的是( )
| A. | 2LSO2和2LCO2 | B. | 9 g水和标准状况下 11.2LCO2 | ||
| C. | 标准状况下1mol氧气和 22.4L水 | D. | 0.1mol氢气和 2.24L氯化氢气体 |
2.如图是乙醇燃料电池的实验装置图,下列有关说法一定正确的是( )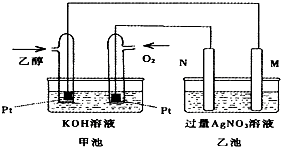

| A. | 若用此装置给铁棒上镀上层银,则N电极改用铁电极,M电极改用银电极 | |
| B. | 甲池中负极的电极反应式为:CH3CH2OH-12e-+3H2O=2CO2+12H+ | |
| C. | 甲池KOH溶液中经过0.05mol电子时,理论上乙池中的M电极质量增加5.04g | |
| D. | M电极上的电极反应式为:Ag++e-=Ag |
9.下列化学反应中,既属于四种基本反应类型又属于氧化还原反应的是( )
| A. | NH4Cl+NaOH$\frac{\underline{\;△\;}}{\;}$NH3↑+H2O+NaCl | B. | 3CO+Fe2O3$\frac{\underline{\;△\;}}{\;}$2Fe+3CO2 | ||
| C. | Cl2+2KBr═Br2+2KCl | D. | NH3+CO2+H2O═NH4HCO3 |
19.铁、铜单质及其化合物应用范围很广. 如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等.
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式2Fe3++Cu=2Fe2++Cu2+.
(2)腐蚀铜板后的混合溶液中,为制取纯净的CuCl2,按如图步骤进行提纯:
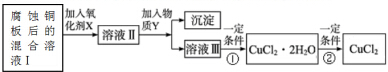
腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol•L-1,已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
25℃时,Ksp[Fe(OH)3]=2.6×10-39
请回答下列问题:
①加入氧化剂的目的是将Fe2+氧化成Fe3+,便于生成Fe(OH)3沉淀而与Cu2+分离.
②最适合作氧化剂X的是C.
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
③加入Y物质,调至pH=4,加入的物质Y可能是CuO[或Cu(OH)2、CuCO3、Cu2(OH)2CO3].此时溶液Ⅲ中的c(Fe3+)=2.6×10-9 mol•L-1.
④最后能不能直接加热CuCl2•2H2O得到CuCl2?不能(填“能”或“不能”).若能,不用回答;若不能,回答该如何操作?应在HCl气流中加热蒸发结晶.
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式2Fe3++Cu=2Fe2++Cu2+.
(2)腐蚀铜板后的混合溶液中,为制取纯净的CuCl2,按如图步骤进行提纯:

腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol•L-1,已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
①加入氧化剂的目的是将Fe2+氧化成Fe3+,便于生成Fe(OH)3沉淀而与Cu2+分离.
②最适合作氧化剂X的是C.
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
③加入Y物质,调至pH=4,加入的物质Y可能是CuO[或Cu(OH)2、CuCO3、Cu2(OH)2CO3].此时溶液Ⅲ中的c(Fe3+)=2.6×10-9 mol•L-1.
④最后能不能直接加热CuCl2•2H2O得到CuCl2?不能(填“能”或“不能”).若能,不用回答;若不能,回答该如何操作?应在HCl气流中加热蒸发结晶.
4.下列说法不正确的是( )
| A. | 电解质溶液导电的过程实际上就是电解的过程 | |
| B. | 利用电解饱和食盐水所得的产物可以生产盐酸 | |
| C. | 铜在酸性环境中易发生析氢腐蚀 | |
| D. | 氢氧燃料电池的负极通入的是氢气 |
 W、X、Y、Z分别为H、C、N、O元素.
W、X、Y、Z分别为H、C、N、O元素.