题目内容
 已知:用惰性电极电解某盐X的溶液,发生的反应为:X+H2O
已知:用惰性电极电解某盐X的溶液,发生的反应为:X+H2O| 电解 |
(1)若组成X的元素均为短周期元素,且A、B均为气体,其在相同条件下体积比为1:1,产物之间可以发生下列反应(变化中的水略去):写出有关反应的离子反应方程式:
①
(2)若A为红色固体,A可以与Y的浓溶液反应生成一种与A摩尔质量相同的气体.
①写出该电解过程中阳极的电极反应式:
②某学生电解一定浓度的X溶液一段时间后,向所得溶液中加入0.lmolA2(OH)2CO3后,恢复到电解前的浓度和pH(不考虑CO2溶解),则电解过程中转移的电子数为
(3)若向X的溶液中加入过量的稀盐酸,产生白色沉淀,且存在如下的转化关系:
I.A+Y(浓)→X+C(气体)+H2O;
Ⅱ.A+Y(稀)→X+D(气体)+H2O;
Ⅲ.M+O2→D(气体)+H2O.
①已知:组成M气体的两种元素质量比为14:3,则检验M的方法是
②在标准状况下,27gA溶于一定浓度的Y溶液时,产生2.8L气体,将装有该气体的量筒倒立于有水的水槽中,再通入
③25℃时,向浓度为0.1mol?L-1的MgCl2、CuCl2、CaCl2混合溶液中通入M气体,最先生成的沉淀的化学式为
已知:Ksp[Mg(OH)2]=1.8xl0-11,Ksp[Cu(OH)2]=2.2xl0-20,Ksp[Ca(OH)2]=5.5xl0-6.
考点:无机物的推断
专题:推断题
分析:(1)若组成X的元素均为短周期元素,且A、B均为气体,其在相同条件下体积比为1:1,应为电解饱和食盐水的反应,则X为NaCl,Y为NaOH,由转化关系可知A为H2,B为Cl2,W为HCl,U为NaClO;
(2)若A为红色固体,应为Cu,A可以与Y的浓溶液反应生成一种与A摩尔质量相同的气体,该气体为SO2,应是电解硫酸铜溶液,则X为CuSO4,B为O2、Y为H2SO4;
(3)若向X的溶液中加入过量的稀盐酸,产生白色沉淀,该沉淀为AgCl,则X为AgNO3,由转化关系可知Y为HNO3,A为Ag,C为NO2,D为NO,M为NH3,以此解答该题.
(2)若A为红色固体,应为Cu,A可以与Y的浓溶液反应生成一种与A摩尔质量相同的气体,该气体为SO2,应是电解硫酸铜溶液,则X为CuSO4,B为O2、Y为H2SO4;
(3)若向X的溶液中加入过量的稀盐酸,产生白色沉淀,该沉淀为AgCl,则X为AgNO3,由转化关系可知Y为HNO3,A为Ag,C为NO2,D为NO,M为NH3,以此解答该题.
解答:
解:(1)若组成X的元素均为短周期元素,且A、B均为气体,其在相同条件下体积比为1:1,应为电解食盐水的反应,则X为NaCl,Y为NaOH,由转化关系可知A为H2,B为Cl2,W为HCl,U为NaClO,
①氯气和氢氧化钠溶液反应生成NaCl、NaClO和水,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
②盐酸和次氯酸钠可发生氧化还原反应生成氯气,反应的离子方程式为2H++Cl-+ClO-=Cl2↑+H2O,故答案为:2H++Cl-+ClO-=Cl2↑+H2O;
(2)若A为红色固体,应为Cu,A可以与Y的浓溶液反应生成一种与A摩尔质量相同的气体,该气体为SO2,应是电解硫酸铜溶液,则X为CuSO4,B为O2、Y为H2SO4,
①电解硫酸铜溶液,阳极发生氧化反应,电极方程式为:4OH--4e-=O2↑+2H2O (或2H2O-4e-=O2↑+4H+),故答案为:4OH--4e-=O2↑+2H2O (或2H2O-4e-=O2↑+4H+);
②电解硫酸铜溶液可能发生如下两个阶段反应:
第一阶段2CuSO4+2H2O
2Cu↓+O2↑+2H2SO4,
第二阶段:2H2O
2H2↑+O2↑,
将碱式碳酸铜化学式改变为2CuO?H2O?CO2,所以加入0.1molCu2(OH)2CO3 就相当于加入0.2molCuO和0.1mol水,
第一阶段:根据铜原子守恒知,电解硫酸铜溶液析出n(Cu)=n(CuO)=0.2mol,转移电子的物质的量=0.2mol×2=0.4mol;
第二阶段:电解生成0.1mol水转移电子的物质的量=0.1mol×2=0.2mol,
所以解过程中共转移的电子数为0.4mol+0.2mol=0.6mol,转移的电子数为0.6NA,
故答案为:0.6NA;
(3)若向X的溶液中加入过量的稀盐酸,产生白色沉淀,该沉淀为AgCl,则X为AgNO3,由转化关系可知Y为HNO3,A为Ag,C为NO2,D为NO,M为NH3,
①检验氨气,可用湿润的红色石蕊试纸靠近盛M的集气瓶口,试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近盛M的集气瓶口,冒白烟),
故答案为:用湿润的红色石蕊试纸靠近盛M的集气瓶口,试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近盛M的集气瓶口,冒白烟);
②A为Ag,B为O2,n(Ag)=
=0.25mol,反应中失去0.25mol电子,根据电子转移守恒,可知消耗的氧气也应得到0.25mol电子,此时水才能恰好充满量筒,则n(O2)=
mol=
mol,
则V(O2)=
mol×22.4L/mol=1.4L,故答案为:1.4.
③Mg(OH)2、Cu(OH)2、Ca(OH)2的结构相同,Cu(OH)2的溶度积更小,其溶解度更小,加入相同的氨水,Cu2+先沉淀生成Cu(OH)2,
故答案为:Cu(OH)2.
①氯气和氢氧化钠溶液反应生成NaCl、NaClO和水,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
②盐酸和次氯酸钠可发生氧化还原反应生成氯气,反应的离子方程式为2H++Cl-+ClO-=Cl2↑+H2O,故答案为:2H++Cl-+ClO-=Cl2↑+H2O;
(2)若A为红色固体,应为Cu,A可以与Y的浓溶液反应生成一种与A摩尔质量相同的气体,该气体为SO2,应是电解硫酸铜溶液,则X为CuSO4,B为O2、Y为H2SO4,
①电解硫酸铜溶液,阳极发生氧化反应,电极方程式为:4OH--4e-=O2↑+2H2O (或2H2O-4e-=O2↑+4H+),故答案为:4OH--4e-=O2↑+2H2O (或2H2O-4e-=O2↑+4H+);
②电解硫酸铜溶液可能发生如下两个阶段反应:
第一阶段2CuSO4+2H2O
| ||
第二阶段:2H2O
| ||
将碱式碳酸铜化学式改变为2CuO?H2O?CO2,所以加入0.1molCu2(OH)2CO3 就相当于加入0.2molCuO和0.1mol水,
第一阶段:根据铜原子守恒知,电解硫酸铜溶液析出n(Cu)=n(CuO)=0.2mol,转移电子的物质的量=0.2mol×2=0.4mol;
第二阶段:电解生成0.1mol水转移电子的物质的量=0.1mol×2=0.2mol,
所以解过程中共转移的电子数为0.4mol+0.2mol=0.6mol,转移的电子数为0.6NA,
故答案为:0.6NA;
(3)若向X的溶液中加入过量的稀盐酸,产生白色沉淀,该沉淀为AgCl,则X为AgNO3,由转化关系可知Y为HNO3,A为Ag,C为NO2,D为NO,M为NH3,
①检验氨气,可用湿润的红色石蕊试纸靠近盛M的集气瓶口,试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近盛M的集气瓶口,冒白烟),
故答案为:用湿润的红色石蕊试纸靠近盛M的集气瓶口,试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近盛M的集气瓶口,冒白烟);
②A为Ag,B为O2,n(Ag)=
| 27g |
| 108g/mol |
| 0.25mol |
| 4 |
| 1 |
| 16 |
则V(O2)=
| 1 |
| 16 |
③Mg(OH)2、Cu(OH)2、Ca(OH)2的结构相同,Cu(OH)2的溶度积更小,其溶解度更小,加入相同的氨水,Cu2+先沉淀生成Cu(OH)2,
故答案为:Cu(OH)2.
点评:本题考查较为综合,涉及无机物的推断,电解以及化学方程式的计算,侧重于学生的分析能力、计算能力的考查,为高频考点和常见题型,注意把握电解的原理和元素化合物知识,难度中等.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
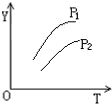 对于密闭容器中的可逆反应:4L(g)?2M(g)+N(g)△H>0,其平衡状态与温度(T)和压强(P1>P2)的关系如图所示.图中y轴是指( )
对于密闭容器中的可逆反应:4L(g)?2M(g)+N(g)△H>0,其平衡状态与温度(T)和压强(P1>P2)的关系如图所示.图中y轴是指( )| A、气体混合物的平均相对分子质量 |
| B、气体混合物的总物质的量浓度 |
| C、L在气体混合物的体积分数 |
| D、气体混合物的密度 |
下列有关糖类、油脂、蛋白质的说法正确的是( )
| A、向鸡蛋清溶液中,加入饱和(NH4)2SO4溶液,有白色沉淀产生,说明蛋白质发生了变性 |
| B、棉花、纸、醋酸纤维的主要成分都是纤维素 |
| C、淀粉、牛油、蛋白质都是天然高分子化合物 |
| D、油脂里饱和烃基的相对含量越大,油脂的熔点越高 |
核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳.核黄素分子的结构为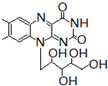 :
:
已知: +H2O
+H2O
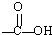 +
+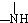 有关核黄素的下列说法中,不正确的是( )
有关核黄素的下列说法中,不正确的是( )
 :
:已知:
 +H2O
+H2O| H+ |
| △ |
 +
+ 有关核黄素的下列说法中,不正确的是( )
有关核黄素的下列说法中,不正确的是( )| A、该化合物的分子式为C17H22N4O6 |
| B、酸性条件下加热水解,有CO2生成 |
| C、酸性条件下加热水解,所得溶液加碱后有NH3生成 |
| D、能发生酯化反应 |
雷雨天闪电时空气中有臭氧(O3)生成.下列说法正确的是( )
| A、O2和O3互为同位素 |
| B、O2和O3的相互转化是物理变化 |
| C、在相同的温度与压强下,等体积的O2和O3含有相同的分子数 |
| D、等物质的量的O2和O3含有相同的质量 |
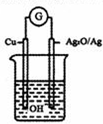 普通水泥在固化过程中自由水分子减少并形成碱性溶液,根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间.此法的原理,反应的总方程式为:2Cu+Ag2O═Cu2O+2Ag.下列有关说法正确的是( )
普通水泥在固化过程中自由水分子减少并形成碱性溶液,根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间.此法的原理,反应的总方程式为:2Cu+Ag2O═Cu2O+2Ag.下列有关说法正确的是( )| A、铜电极附近有黑色沉淀生成 |
| B、负极的电极反应式为2Cu+2OH--2e-═Cu2O+H2O |
| C、测量原理示意图中,电流方向从Cu经过导线流向Ag2O |
| D、电池工作时,溶液中OH-向正极移动 |
下列依据相关数据作出的推理和判断中,不正确的是( )
| A、依据相对分子质量的数据,推测乙醇和丙烷沸点的相对高低 |
| B、依据溶解度的数据,选择用重结晶的方法可将粗苯甲酸提纯 |
| C、依据沸点的数据,判断用分馏的方法从石油中获取汽油和煤油等 |
| D、依据燃烧热的数据、热化学方程式和盖斯定律,可计算一些反应的反应热 |
1L0.1mol?L-1 AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极增重2.16g时,下列判断正确的是(设电解按理论进行,溶液不蒸发)( )
| A、转移的电子数是1.204×1022 |
| B、阳极上产生112mLO2(标准状况) |
| C、溶液的浓度变化为0.08mol?L-1 |
| D、反应中有0.01molAg被氧化 |
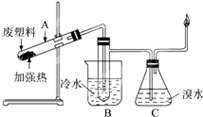 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如下表
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如下表