题目内容
18.下列分子中所有碳原子肯定不在同一平面上的是( )| A. | 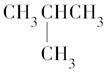 | B. | CH3CH=CHCH3 | C. | CH2=CHCH2CH3 | D. | 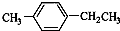 |
分析 在常见的有机化合物中,甲烷是正四面体结构,乙烯和苯都是平面型结构,乙炔是直线型结构,以此解答该题.
解答 解:A.为烷烃,具有甲烷的结构特点,则所有碳原子肯定不在同一平面上,故A选;
B.碳碳双键为平面形结构,与碳碳双键直接相连的原子在同一个平面上,则所有碳原子肯定在同一平面上,故B不选;
C.与碳碳双键直接相连的原子在同一个平面上,结合三点共面原则,可能在同一个平面上,故C不选;
D.苯环为平面形结构,与苯环直接相连的原则在同一个平面上,结合三点共面原则,可能在同一个平面上,故D不选.
故选A.
点评 本题考查有机化合物的结构特点,为高考常见题型和高频考点,侧重考查学生的分析能力,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构,难度不大.

练习册系列答案
相关题目
18.下列关于烃性质的说法中正确的是( )
| A. | 乙烯可以与酸性高锰酸钾溶液反应,因此可以用酸性高锰酸钾溶液除去乙烷中混有的乙烯 | |
| B. | 溴乙烷可以通过乙烯与溴化氢加成得到,也可以通过乙烷与溴发生取代反应制备 | |
| C. | 区分甲苯和苯可以使用酸性高锰酸钾溶液,也可以用溴的四氯化碳溶液 | |
| D. | 鉴别己烯中是否混有少量甲苯,正确的实验方法是可以加足量溴的四氯化碳溶液,然后再加入酸性高锰酸钾溶液 |
9.某同学为了探究锌与盐酸反应过程中的速率变化,在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值):
(3)哪一时间段反应速率最大C,原因是因反应为放热反应,温度升高,反应速率增大.
A.0:1mim B.1:2mimC.2:3mim D.3:4mim E.4:5mim
(4)在2:3mim时间段,以盐酸溶液浓度的变化来表示该反应的速率,结果为(溶液体积不变)
0.1mol/(L•min).
(5)为减缓反应速率又不减少产生氢气的量,可在盐酸中加入:AB.
A.蒸馏水B.NaCl溶液C.NaNO3溶液D.CuSO4溶液E.Na2CO3溶液.
| 时间(mim) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(ML) | 50 | 120 | 232 | 290 | 310 |
A.0:1mim B.1:2mimC.2:3mim D.3:4mim E.4:5mim
(4)在2:3mim时间段,以盐酸溶液浓度的变化来表示该反应的速率,结果为(溶液体积不变)
0.1mol/(L•min).
(5)为减缓反应速率又不减少产生氢气的量,可在盐酸中加入:AB.
A.蒸馏水B.NaCl溶液C.NaNO3溶液D.CuSO4溶液E.Na2CO3溶液.
6.硫酸铜晶体中结晶水含量测定,需用的仪器有( )
| A. | 容量瓶 | B. | 分液漏斗 | C. | 干燥器 | D. | 滴定管 |
13.下列离子方程式正确的是( )
| A. | 向氢氧化亚铁中加入足量稀硝酸:Fe(OH)2+2H+═Fe2++2H2O | |
| B. | 向 NaClO 溶液中通入过量SO2气体:ClO-+H2O+SO2═HClO+HSO3- | |
| C. | 向偏铝酸钠溶液中加入碳酸氢钠:AlO2-+3HCO3-═Al(OH)3↓+3CO2↑ | |
| D. | 向NH4HCO3溶液中加入过量NaOH溶液:NH4++HCO3-+2OH-═NH3•H2O+H2O+CO32- |
3.下列说法中正确的是( )
| A. | 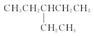 在核磁共振氢谱中有7个吸收峰 在核磁共振氢谱中有7个吸收峰 | |
| B. | 红外光谱图只能确定有机物中所含官能团的种类和数目 | |
| C. | 质谱法不能用于相对分子质量的测定 | |
| D. | 核磁共振氢谱、红外光谱和质谱都可用于分析有机物结构 |
7.下列属于氧化还原反应同时能量的变化符合如图的是( )
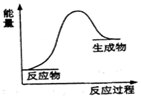

| A. | Ba(OH)2•8H2O与NH4Cl反应 | |
| B. | 铝与稀盐酸 | |
| C. | 灼热的炭与水蒸气生成一氧化碳和氢气的反应 | |
| D. | 煤与O2的燃烧反应 |
12.据报导,我国已研制出“可充室温钠一二氧化碳电池”,电极材料为钠金属片和碳纳米管,电解液为高氯酸钠一四甘醇二甲醚,电池总反应为:4Na+3CO2 $?_{充电}^{放电}$2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上.下列叙述不正确的是( )
| A. | 放电时钠金属片发生氧化反应 | |
| B. | 充电时碳纳米管接直流电源的正极 | |
| C. | 放电时每消耗3molCO2,转移12 mol电子 | |
| D. | 充电时的阳极反应为C+2Na2CO3-4e-=3CO2↑+4Na+ |