题目内容
某化学学习小组对铝与酸和碱的反应进行探究,过程如下.
实验Ⅰ:
(1)取形状、大小均相同的铝丝分别与等体积的、pH相同的盐酸、稀硫酸反应,随反应进行,盐酸中生成气体的速率明显比硫酸中生成气体的速率快,对此原因,你认为合理的猜测是下列的 (填写相应的字母).
a.盐酸的物质的量浓度大于硫酸的物质的量浓度 b.Cl-能促进此反应的进行
c.SO42-能抑制此反应的进行 d.硫酸使铝发生钝化
(2)为了探究反应速率不同的原因,请你根据所提供的药品,填写实验方案中的空白部分.
药品:氯化铝固体、硫酸铝固体、硫酸铜固体、氯化铜固体、6mol/L盐酸、3mol/L硫酸、,18.4mol/L硫酸、5mol/L硝酸.
方案:取两支试管,首先同时分别加入形状、大小均相同的铝丝和等体积的 (填写相应的试剂,下同),然后再向其中的一支试管中加入适量的 固体并振荡使固体溶解,观察实验现象.
实验探究:略.
实验Ⅱ:
取足量的形状、质量均相同的铝丝分别与等体积的6mol/L的盐酸、6mol/L氢氧化钠溶液反应,待反应停止后取出剩余的铝丝洗净、干燥、称量,剩余铝丝的质量关系是前者 后者(填“大于”或“小于”或“等于”);观察反应后的液体,发现铝与盐酸反应后所得的液体是黑色浑浊的,试管底部有少量黑色沉淀,对此现象,同学们进行了如下探究:
(1)提出猜想
同学们查找资料后获得如下信息:工业上用电解法冶炼铝所用的原料氧化铝是从铝土矿中提取的,所以得到的氧化铝中可能还含有微量的氧化铁和二氧化硅两种杂质,据此,同学们提出如下猜想:
猜想1:此黑色固体是铁单质,可能是电解得到的铝与杂质反应生成的,相应的化学反应方程式为 ;
猜想2:此黑色固体是硅单质,是电解得到的铝与二氧化硅反应生成的;
猜想3:此黑色固体是铝单质,是铝与盐酸反应时因反应过快而变成粉末分散到溶液中;
猜想4:此黑色固体可能是上述若干种单质组成的混合物.
(2)设计实验方案并完成相关实验:
为了探究少量黑色沉淀的成分,将反应后所得的液体进行 、 (填基本操作),分别取少量固体置于两支试管中,完成下列实验:
①向其中的一支试管中加入足量的稀盐酸,观察固体是否溶解.实验时发现固体完全溶解,证明猜想 一定不正确(填“1”、“2”、“3”、“4”).
②向另一试管中加入足量的氢氧化钠溶液,观察固体是否溶解.实验时发现固体完全溶解,证明猜想 一定不正确(填“1”、“2”、“3”、“4”).
(3)得出结论
综合实验①②的现象,可推知猜想 (填“1”、“2”、“3”、“4”)是正确的,固体溶解在氢氧化钠溶液中的离子方程式为: .
实验Ⅰ:
(1)取形状、大小均相同的铝丝分别与等体积的、pH相同的盐酸、稀硫酸反应,随反应进行,盐酸中生成气体的速率明显比硫酸中生成气体的速率快,对此原因,你认为合理的猜测是下列的
a.盐酸的物质的量浓度大于硫酸的物质的量浓度 b.Cl-能促进此反应的进行
c.SO42-能抑制此反应的进行 d.硫酸使铝发生钝化
(2)为了探究反应速率不同的原因,请你根据所提供的药品,填写实验方案中的空白部分.
药品:氯化铝固体、硫酸铝固体、硫酸铜固体、氯化铜固体、6mol/L盐酸、3mol/L硫酸、,18.4mol/L硫酸、5mol/L硝酸.
方案:取两支试管,首先同时分别加入形状、大小均相同的铝丝和等体积的
实验探究:略.
实验Ⅱ:
取足量的形状、质量均相同的铝丝分别与等体积的6mol/L的盐酸、6mol/L氢氧化钠溶液反应,待反应停止后取出剩余的铝丝洗净、干燥、称量,剩余铝丝的质量关系是前者
(1)提出猜想
同学们查找资料后获得如下信息:工业上用电解法冶炼铝所用的原料氧化铝是从铝土矿中提取的,所以得到的氧化铝中可能还含有微量的氧化铁和二氧化硅两种杂质,据此,同学们提出如下猜想:
猜想1:此黑色固体是铁单质,可能是电解得到的铝与杂质反应生成的,相应的化学反应方程式为
猜想2:此黑色固体是硅单质,是电解得到的铝与二氧化硅反应生成的;
猜想3:此黑色固体是铝单质,是铝与盐酸反应时因反应过快而变成粉末分散到溶液中;
猜想4:此黑色固体可能是上述若干种单质组成的混合物.
(2)设计实验方案并完成相关实验:
为了探究少量黑色沉淀的成分,将反应后所得的液体进行
①向其中的一支试管中加入足量的稀盐酸,观察固体是否溶解.实验时发现固体完全溶解,证明猜想
②向另一试管中加入足量的氢氧化钠溶液,观察固体是否溶解.实验时发现固体完全溶解,证明猜想
(3)得出结论
综合实验①②的现象,可推知猜想
考点:探究影响化学反应速率的因素
专题:实验设计题
分析:实验I:(1)比较盐酸和稀硫酸的不同点进行猜测;
(2)取酸和具有和酸不同离子的盐进行实验比较分析;
实验II:根据反应方程式判断;
(1)根据铝热反应写出反应方程式;
(2)根据操作的目的是将固体与液体分离来选择合适的实验操作;根据实验现象证明猜想;
(3)根据实验不同现象判断正误并写出氧化铝和氢氧化钠反应的离子方程式.
(2)取酸和具有和酸不同离子的盐进行实验比较分析;
实验II:根据反应方程式判断;
(1)根据铝热反应写出反应方程式;
(2)根据操作的目的是将固体与液体分离来选择合适的实验操作;根据实验现象证明猜想;
(3)根据实验不同现象判断正误并写出氧化铝和氢氧化钠反应的离子方程式.
解答:
解:实验I:(1)取形状、大小均相同的铝丝分别与等体积的、PH相同的盐酸、稀硫酸反应,不同点是盐酸中含有氯离子,硫酸中含有硫酸根离子,所以猜测是氯离子促进反应,硫酸根离子抑制反应,
故选bc;
(2)选取酸,然后向酸中加入含有不同阴离子的盐并振荡使固体溶解,观察实验现象,从而确定影响因素,
故答案为:3mol/LH2SO4、氯化铝固体(或6mol/LHCl、硫酸铝固体);
实验II:由反应2Al+6HCl=2AlCl3+H2↑ 2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知,
消耗相同物质的量的盐酸和氢氧化钠,加盐酸溶液的试管中参加反应的铝少,剩余的铝多,
故答案为:大于;
(1)在高温条件下,铝和氧化铁反应生成铁和氧化铝,反应方程式为:2Al+Fe2O3
2Fe+Al2O3,
故答案为:2Al+Fe2O3
2Fe+Al2O3 .
(2)为了探究少量黑色沉淀的成分,故需将固体与溶液分离,采取的操作应为过滤,由于固体上有溶液残留,故还应洗涤,故答案为:过滤,洗涤;
①向其中的一支试管中加入足量的稀盐酸,实验时发现固体完全溶解,说明固体都是金属单质,所以证明猜想 2一定不正确,故答案为:2;
②向另一试管中加入足量的氢氧化钠溶液,实验时发现固体完全溶解,铝和硅都能与氢氧化钠反应,根据实验现象证明猜想 1一定不正确,故答案为:1;
(3)综合实验①②的现象,可推知猜想3是正确的;铝和氢氧化钠反应生成偏铝酸钠和氢气,
故答案为:3;2Al+2OH-+2H2O=2AlO2-+3H2↑.
故选bc;
(2)选取酸,然后向酸中加入含有不同阴离子的盐并振荡使固体溶解,观察实验现象,从而确定影响因素,
故答案为:3mol/LH2SO4、氯化铝固体(或6mol/LHCl、硫酸铝固体);
实验II:由反应2Al+6HCl=2AlCl3+H2↑ 2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知,
消耗相同物质的量的盐酸和氢氧化钠,加盐酸溶液的试管中参加反应的铝少,剩余的铝多,
故答案为:大于;
(1)在高温条件下,铝和氧化铁反应生成铁和氧化铝,反应方程式为:2Al+Fe2O3
| ||
故答案为:2Al+Fe2O3
| ||
(2)为了探究少量黑色沉淀的成分,故需将固体与溶液分离,采取的操作应为过滤,由于固体上有溶液残留,故还应洗涤,故答案为:过滤,洗涤;
①向其中的一支试管中加入足量的稀盐酸,实验时发现固体完全溶解,说明固体都是金属单质,所以证明猜想 2一定不正确,故答案为:2;
②向另一试管中加入足量的氢氧化钠溶液,实验时发现固体完全溶解,铝和硅都能与氢氧化钠反应,根据实验现象证明猜想 1一定不正确,故答案为:1;
(3)综合实验①②的现象,可推知猜想3是正确的;铝和氢氧化钠反应生成偏铝酸钠和氢气,
故答案为:3;2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评:本题考查了铝及其化合物性质的实验,难度不大,注意铝和氢氧化钠溶液反应方程式的书写,水作反应物参加反应.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
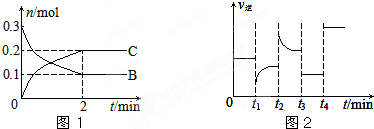
一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?xC(g)△H<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2
下列有关说法正确的是( )
下列有关说法正确的是( )

| A、x=2,反应开始2 min内,v(B)=0.1 mol/(L?min) |
| B、t3时可能是减小压强,平衡不移动;t4时可能是使用催化剂,c(B)不变 |
| C、t2时改变的条件可能是增大c(C),B的转化率增大 |
| D、t1时改变的条件可能是降温,A(s)的质量增加 |
一定质量的甲烷燃烧后的产物为CO、CO2和水蒸气,此混合气体质量为49.6g,当其缓慢经过无水CaCl2时,CaCl2增重25.2g.原混合气体中CO2的质量为( )
| A、12.5g |
| B、13.2g |
| C、19.7g |
| D、24.4g |
一定温度下,向a mol?L-1 NaOH溶液中通入足量的二氧化碳,下列说法正确的是( )
| A、溶液中Kw减小 |
| B、溶液中的CO32-离子浓度一直增大 |
| C、微热反应后的溶液,溶液的pH会升高 |
| D、当恰好生成NaHCO3时,溶液中离子浓度大小存在以下关系:c(Na+)+c(H-)═c(HCO3)+c(OH-) |
下列关于一些常见物质和实验用品的说法中,正确的是( )
| A、用NaOH标准溶液滴定未知浓度的硫酸要用到:石蕊试剂、碱式滴定管、锥形瓶 |
| B、棉、丝、毛皮以及合成纤维完全燃烧只生成H2O和CO2 |
| C、油脂在碱的作用下可发生水解,工业上利用该反应生产肥皂 |
| D、塑料、钢化玻璃、玻璃钢都是硅酸盐制品 |
