题目内容
17.已知吡啶(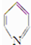 )与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
)与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
| A. | M能使酸性高锰酸钾溶液褪色 | |
| B. | 1molM与金属钠反应,消耗2mol Na | |
| C. | 1mol磷酸吡醛与NaOH溶液反应,最多消耗3mol NaOH | |
| D. | M与足量H2反应后所得有机物的分子式为C8H17O3N |
分析 A.M中含-OH、-CHO均可被氧化;
B.磷酸吡醛中3个-OH均与Na反应;
C.磷酸吡醛水解生成M和磷酸,磷酸、吡啶环上的羟基均能与NaOH溶液反应;
D.M中-CHO及环状结构均与氢气发生加成反应.
解答 解:A.醇羟基、醛基等都能使酸性高锰酸钾溶液褪色,故A正确;
B.1 mol磷酸吡醛中含有2 mol-OH,故消耗金属钠2 mol,故B正确;
C.1 mol磷酸吡醛水解生成1 mol M和1 mol磷酸,又吡啶与苯环性质相似,故直接连在吡啶环上的羟基也能与NaOH溶液反应,即1 mol磷酸吡醛最多消耗4 mol NaOH,故C错误;
D.根据M的分子式为C8H9O3N,1 mol M可以消耗4 mol H2,故生成物分子式为C8H17O3N,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质的关系为解答的关键,侧重醇、醛性质的考查,注意吡啶与苯环性质相似,题目难度不大.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
7.某原电池结构如图所示,下列有关该原电池的说法不正确的是( )
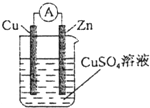

| A. | 铜棒为正极 | B. | 锌棒发生氧化反应 | ||
| C. | 电流从铜棒经外电路流向锌棒 | D. | 锌棒质量增加 |
8.只用一种试剂鉴别NH4Cl、KCl、Na2SO3、和(NH4)2SO4,该试剂是( )
| A. | BaCl2溶液 | B. | NaOH溶液 | C. | Ba(OH)2溶液 | D. | AgNO3溶液 |
9.将2mol A气体和1mol B气体在固定体积的密闭容器中混合并在一定条件下发生如下反应并达到平衡状态:2A(g)+B(g)?2C(g),此反应为放热反应.下列能增大正、逆反应速率的方法是:
(1)再充入1mol A气体;(2)充入2mol的惰性气体;(3)加入正催化剂;(4)升高温度;(5)移走部分C气体.
其中正确的是( )
(1)再充入1mol A气体;(2)充入2mol的惰性气体;(3)加入正催化剂;(4)升高温度;(5)移走部分C气体.
其中正确的是( )
| A. | (1)(3)(5) | B. | (1)(3)(4) | C. | (1)(2)(4)(5) | D. | (1)(2)(3)(4)(5) |
1.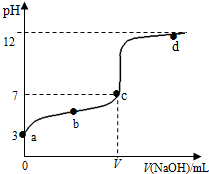 在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:
在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:
(1)实验中的指示剂最好使用酚酞;
(2)当V (NaOH)=20.00mL时,请写出溶液中主要存在的两种平衡体系是A-+H2O?HA+OH-、H2O?H++OH-;
溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+);
(3)a、b、c、d四点对应溶液中水的电离程度由大到小的顺序是c>b>a>d.
(4)该温度下,滴定曲线上c点时HA的电离平衡常数Ka=$\frac{1{0}^{-7}V}{20-V}$.(用含V的代数简式表示)
 在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:
在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:| V(NaOH)mL | 0.00 | 10.00 | 18.00 | 19.80 | 19.98 | 20.00 | 20.02 | 20.20 | 22.00 | 40.00 |
| pH | 3.0 | 4.7 | 5.7 | 6.7 | 7.7 | 8.7 | 9.7 | 10.7 | 11.7 | 12.5 |
(2)当V (NaOH)=20.00mL时,请写出溶液中主要存在的两种平衡体系是A-+H2O?HA+OH-、H2O?H++OH-;
溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+);
(3)a、b、c、d四点对应溶液中水的电离程度由大到小的顺序是c>b>a>d.
(4)该温度下,滴定曲线上c点时HA的电离平衡常数Ka=$\frac{1{0}^{-7}V}{20-V}$.(用含V的代数简式表示)
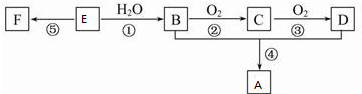
 ,反应类型加聚反应.
,反应类型加聚反应.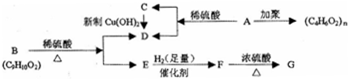
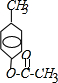 ;
;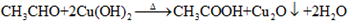 ,反应类型氧化反应;F→G
,反应类型氧化反应;F→G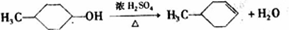 ,反应类型消去反应.
,反应类型消去反应.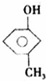 、
、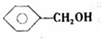 .
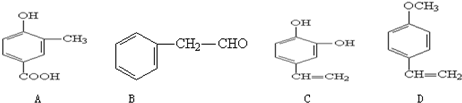
.
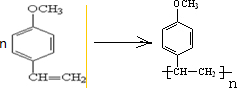
 .
.