题目内容
利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,下图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图.当电池工作时,有关说法正确的是( )
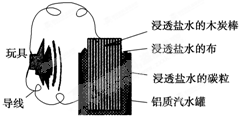

| A、铝罐将逐渐被腐蚀 |
| B、碳粒和炭棒上发生的反应为O2+4e-═2O2- |
| C、炭棒应与玩具电机的负极相连 |
| D、该电池工作一段时间后炭棒和碳粒的质量会减轻 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该装置构成原电池,铝易失电子作负极,碳作正极,负极上电极反应式为:Al-3e-═Al3+,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-═4OH-,以此解答该题.
解答:
解:A.该装置构成原电池,铝易失电子作负极,负极上铝失电子生成铝离子,所以铝罐逐渐被腐蚀,故A正确;
B.碳棒作正极,正极上氧气得电子生成氢氧根离子,电极反应式为O2+2H2O+4e-═4OH-,故B错误;
C.碳棒作正极,应该与玩具电机的正极相连形成闭合回路,故C错误;
D.正极上是氧气得电子,炭粒和碳棒不参加反应,所以其质量不变,故D错误;
故选A.
B.碳棒作正极,正极上氧气得电子生成氢氧根离子,电极反应式为O2+2H2O+4e-═4OH-,故B错误;
C.碳棒作正极,应该与玩具电机的正极相连形成闭合回路,故C错误;
D.正极上是氧气得电子,炭粒和碳棒不参加反应,所以其质量不变,故D错误;
故选A.
点评:本题考查了金属的腐蚀与防护,为高频考点,明确原电池原理是解本题关键,难点是电极反应式的书写,注意结合电解质溶液酸碱性书写,难度中等.

练习册系列答案
相关题目
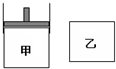 有两只密闭容器甲和乙.甲容器有一个可以移动的活塞能使容器内保持恒压,乙容器能保持恒容.起始时向这两个容器中分别充入等物质的量的体积比为2:1的M和N的混合气体,并使甲和乙容积相等(如右图所示).在保持400℃的条件下使之发生如下反应:2M(g)+N(g)?2Q(g),并达到平衡.下列说法正确的是( )
有两只密闭容器甲和乙.甲容器有一个可以移动的活塞能使容器内保持恒压,乙容器能保持恒容.起始时向这两个容器中分别充入等物质的量的体积比为2:1的M和N的混合气体,并使甲和乙容积相等(如右图所示).在保持400℃的条件下使之发生如下反应:2M(g)+N(g)?2Q(g),并达到平衡.下列说法正确的是( )| A、甲容器达到平衡时所需的时间比乙容器长 |
| B、平衡时甲容器中M的转化率比乙容器小 |
| C、平衡后,若向两容器中通入数量不多的等物质的量的氩气,甲容器中化学平衡向逆反应方向移动,乙容器中化学平衡不移动 |
| D、平衡后,若向两容器中通入等物质的量的原反应气体,达到平衡时,甲容器的混合气体中Q的体积分数变小,乙容器的混合气体中Q的体积分数增大 |
某温度下,在一固定体积的密闭容器中,进行如下化学反应:H2(g)+I2(g)?2HI(g),下列情况能说明该反应一定达到平衡状态的是( )
| A、混合气体的颜色不再改变 |
| B、混合气体的压强不再改变 |
| C、单位时间内拆开1 mol H-H键,同时生成2 mol H-I键 |
| D、混合气体的密度不再改变 |
在Cu-Zn-H2SO4电池中失去电子做负极的极是( )
| A、Cu |
| B、Zn |
| C、H2SO4 |
| D、无法确定 |
已知:C(s)+O2(g)=CO2(g)△H1
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
4Fe(s)+3O2(g)=2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
4Fe(s)+3O2(g)=2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
| A、△H1>0,△H2>0 |
| B、△H3<0,△H4>0 |
| C、△H3=△H1-△H2 |
| D、△H4=2△H5-3△H3 |
下列有关实验的说法不正确的是( )
| A、当沉淀的颗粒较大时,也可用倾析法将固体和溶液分离 |
| B、结晶时,若溶质的溶解度越大,或溶液的浓度越高、或溶剂的蒸发速度越快,析出的晶粒就越细小 |
| C、利用硝酸和硝酸银溶液可区分工业盐和食盐 |
| D、制备阿司匹林时可能混有少量的聚合物杂质,可用碳酸氢钠溶液进行提纯 |