题目内容
(14分)肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O)。CO(NH2) + 2NaOH + NaClO = Na2CO3 + N2H4·H2O + NaCl
实验一:制备NaClO溶液
(1)将氯气通入到盛有NaOH的锥形瓶中,锥形瓶中发生反应的离子方程式是 ;
实验二:制取水合肼(实验装置如图所示)

控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。(已知:N2H4·H2O + 2NaClO=N2↑ + 3H2O + 2NaCl)
(2)分液漏斗中的溶液是 (填标号A或B);
A.NaOH和NaClO混合溶液
B.CO (NH2) 2溶液
选择的理由是 ;
实验三:测定馏分中肼含量水合肼具有还原性,可以生成氮气。测定水合肼的质量分数可采用下列步骤:
a.称取馏分5.000g,加入适量NaHCO3固体,经稀释、转移、定容等步骤,配制250mL溶液。
b.移取25.00 mL于锥形瓶中,加入10mL水,摇匀.
c.用0.2000mol/L碘溶液滴定至溶液出现微黄色且半分钟内不消失,滴定过程中,溶液的pH保持在6.5左右。记录消耗碘的标准液的体积。
d.进一步操作与数据处理
(3)水合肼与碘溶液反应的化学方程式 ;滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是 。
(4)滴定时,碘的标准溶液盛放在 滴定管中(选填:“酸式”或“碱式”);若本次滴定消耗碘的标准溶液为18.00mL,馏分中水合肼(N2H4·H2O)的质量分数为 (保留三位有效数字);
(5)为获得更可靠的滴定结果,步骤d中进一步操作主要是: 。
(1)Cl2+ 2OH—=ClO— + Cl— + H2O (2分)
(2)A(2分)如果次氯酸钠溶液装在烧瓶中,反应生成的水合肼会被次氯酸钠氧化(2分)
(3)N2H4·H2O + 2I2 = N2↑+ 4HI + H2O (2分)生成的HI与NaHCO3 反应 (1分)
(4)酸式(1分) 18.0%或0.180(2分)
(5)重复步骤b和c 2~3次,依据测得的结果,取平均值。(2分)(只答重复步骤b和c 2~3次也可以给分)
【解析】
试题分析:(1)氯气与氢氧化钠溶液反应的离子方程式为Cl2+ 2OH—=ClO— + Cl— + H2O;
(2)由于水合肼易被次氯酸钠氧化,因此如果次氯酸钠溶液装在烧瓶中,反应生成的水合肼会被次氯酸钠氧化,所以分液漏斗中的溶液是NaOH和NaClO混合溶液,答案选A。
(3)碘具有氧化性,能氧化水合肼生成氮气,反应的化学方程式为N2H4·H2O + 2I2 = N2↑+ 4HI + H2O;生成的氢碘酸是强酸,能与次氯酸钠溶液反应,从而可以控制溶液的pH值。
(4)碘水显酸性,因此滴定时,碘的标准溶液盛放在酸式滴定管中;消耗碘的物质的量是0.2000mol/L ×0.018L=0.0036mol,则水合肼的物质的量是0.0018mol,质量是0.0018mol×50g/mol=0.09g,则馏分中水合肼(N2H4·H2O)的质量分数为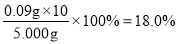 ;
;
(5)为获得更可靠的滴定结果,步骤d中进一步操作主要是重复步骤b和c 2~3次,依据测得的结果,取平均值。
考点:考查物质制备实验方案设计与探究

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案下列操作能达到实验目的的是
目 的 | 操 作 | |
A | 确定某卤代烃为氯代烃 | 取某卤代烃少许与NaOH溶液共热后再加盐酸酸化, 然后加AgNO3溶液,有白色沉淀 |
B | 配制银氨溶液 | 在硝酸银溶液中滴加稀氨水至沉淀恰好消失 |
C | 提取碘水中的碘 | 将碘水倒入分液漏斗,加入适量乙醇,振荡后静置 |
D | 确定蔗糖是否发生水解 | 取2 mL水解液滴加少量新制的Cu(OH)2悬浊液,加热 |




