题目内容
有A、B、C、D、E、F六种前四周期元素,原子序数依次增大且它们原子序数之和为77.A的一种核素没有中子,B、C、D三种元素的基态原子具有相同的能层和能级,且I1(B)<I1(D)<I1(C),(I1表示第一电离能),其中基态C原子的2p轨道处于半充满状态,且C2D与BD2互为等电子体.E为周期表第四周期中未成对电子数最多的元素,请回答下列问题:
(1)在上述六种元素中,电负性最大的是 (填元素符号).
(2)元素E在周期表中的位置 .
(3)基态F原子的核外电子排布式为 .
(4)FC的晶体结构与单晶硅相似,在FC晶体中,每个F原子与 个C原子相连,与同一个F原子相连的C原子构成的空间构型为 .
(5)AC3是一种弱酸,它可由C2A4与ACD2反应制得,反应方程式为 .
(6)A与D可形成一种团簇粒子A3D+(A2D)3,光谱分析粒子中A2D分子具有相同的环境,请画出该团簇粒子的空间结构 .
(1)在上述六种元素中,电负性最大的是
(2)元素E在周期表中的位置
(3)基态F原子的核外电子排布式为
(4)FC的晶体结构与单晶硅相似,在FC晶体中,每个F原子与
(5)AC3是一种弱酸,它可由C2A4与ACD2反应制得,反应方程式为
(6)A与D可形成一种团簇粒子A3D+(A2D)3,光谱分析粒子中A2D分子具有相同的环境,请画出该团簇粒子的空间结构
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:有A、B、C、D、E、F六种前四周期元素,原子序数依次增大且它们原子序数之和为77,A的一种核素没有中子,则A是H元素;
B、C、D三种元素的基态原子具有相同的能层和能级,基态C原子的2p轨道处于半充满状态,则C是N元素,
I1(B)<I1(D)<I1(C),(I1表示第一电离能),且C2D与BD2互为等电子体,则B是C、D是O元素;
E为周期表第四周期中未成对电子数最多的元素,则E是Cr元素,这几种元素原子序数之和为77,则F是Ga元素,
(1)同一周期元素,电负性随着原子序数增大而增大,同一主族元素,电负性随着原子序数增大而减小;
(2)E位于第四周期第VIB族;
(3)基态F原子核外有31个电子,根据构造原理书写其核外电子排布式;
(4)GaN的晶体结构和单晶硅相似,每个原子形成四个共价键;与同一个F原子相连的C原子构成的空间构型为正四面体;
(5)HN3是一种弱酸,它可由N2H4与HNO2反应制得,二者反应生成叠氮酸、水;
(6)H与O可形成一种团簇粒子H3O+(H2O)3,H3O+的空间构型为三角锥形,O原子位于锥顶,3个H原子位于锥底,3个水分子所处位置相同,所以3个水分子分别与3个H原子形成氢键.
B、C、D三种元素的基态原子具有相同的能层和能级,基态C原子的2p轨道处于半充满状态,则C是N元素,
I1(B)<I1(D)<I1(C),(I1表示第一电离能),且C2D与BD2互为等电子体,则B是C、D是O元素;
E为周期表第四周期中未成对电子数最多的元素,则E是Cr元素,这几种元素原子序数之和为77,则F是Ga元素,
(1)同一周期元素,电负性随着原子序数增大而增大,同一主族元素,电负性随着原子序数增大而减小;
(2)E位于第四周期第VIB族;
(3)基态F原子核外有31个电子,根据构造原理书写其核外电子排布式;
(4)GaN的晶体结构和单晶硅相似,每个原子形成四个共价键;与同一个F原子相连的C原子构成的空间构型为正四面体;
(5)HN3是一种弱酸,它可由N2H4与HNO2反应制得,二者反应生成叠氮酸、水;
(6)H与O可形成一种团簇粒子H3O+(H2O)3,H3O+的空间构型为三角锥形,O原子位于锥顶,3个H原子位于锥底,3个水分子所处位置相同,所以3个水分子分别与3个H原子形成氢键.
解答:
解:有A、B、C、D、E、F六种前四周期元素,原子序数依次增大且它们原子序数之和为77,A的一种核素没有中子,则A是H元素;
B、C、D三种元素的基态原子具有相同的能层和能级,基态C原子的2p轨道处于半充满状态,则C是N元素,
I1(B)<I1(D)<I1(C),(I1表示第一电离能),且C2D与BD2互为等电子体,则B是C、D是O元素;
E为周期表第四周期中未成对电子数最多的元素,则E是Cr元素,这几种元素原子序数之和为77,则F是Ga元素,
(1)同一周期元素,电负性随着原子序数增大而增大,同一主族元素,电负性随着原子序数增大而减小,所以这几种元素中电负性最大的是O元素,故答案为:O;
(2)E原子核外有4个电子层,价电子数是6,价电子包含3d、4s电子,所以位于第四周期第VIB族,故答案为:第四周期第VIB族;
(3)基态F原子核外有31个电子,根据构造原理知其核外电子排布式为1s22s22p63s23p63d104s24p1 ,
故答案为:1s22s22p63s23p63d104s24p1 ;
(4)GaN的晶体结构和单晶硅相似,每个原子形成四个共价键,所以每个F原子与4个C原子相连;与同一个F原子相连的C原子构成的空间构型为正四面体,故答案为:4;正四面体;
(5)HN3是一种弱酸,它可由N2H4与HNO2反应制得,二者反应生成叠氮酸、水,反应方程式为N2H4+HNO2=HN3+2H2O,故答案为:N2H4+HNO2=HN3+2H2O;
(6)H与O可形成一种团簇粒子H3O+(H2O)3,H3O+的空间构型为三角锥形,O原子位于锥顶,3个H原子位于锥底,3个水分子所处位置相同,所以3个水分子分别与3个H原子形成氢键,其结构为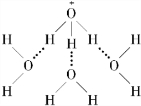 ,故答案为:
,故答案为: .
.
B、C、D三种元素的基态原子具有相同的能层和能级,基态C原子的2p轨道处于半充满状态,则C是N元素,
I1(B)<I1(D)<I1(C),(I1表示第一电离能),且C2D与BD2互为等电子体,则B是C、D是O元素;
E为周期表第四周期中未成对电子数最多的元素,则E是Cr元素,这几种元素原子序数之和为77,则F是Ga元素,
(1)同一周期元素,电负性随着原子序数增大而增大,同一主族元素,电负性随着原子序数增大而减小,所以这几种元素中电负性最大的是O元素,故答案为:O;
(2)E原子核外有4个电子层,价电子数是6,价电子包含3d、4s电子,所以位于第四周期第VIB族,故答案为:第四周期第VIB族;
(3)基态F原子核外有31个电子,根据构造原理知其核外电子排布式为1s22s22p63s23p63d104s24p1 ,
故答案为:1s22s22p63s23p63d104s24p1 ;
(4)GaN的晶体结构和单晶硅相似,每个原子形成四个共价键,所以每个F原子与4个C原子相连;与同一个F原子相连的C原子构成的空间构型为正四面体,故答案为:4;正四面体;
(5)HN3是一种弱酸,它可由N2H4与HNO2反应制得,二者反应生成叠氮酸、水,反应方程式为N2H4+HNO2=HN3+2H2O,故答案为:N2H4+HNO2=HN3+2H2O;
(6)H与O可形成一种团簇粒子H3O+(H2O)3,H3O+的空间构型为三角锥形,O原子位于锥顶,3个H原子位于锥底,3个水分子所处位置相同,所以3个水分子分别与3个H原子形成氢键,其结构为
 ,故答案为:
,故答案为: .
.
点评:本题考查位置结构性质相互关系及应用,涉及氢键、晶体空间构型、核外电子排布、电负性等知识点,这些都是高考高频点,熟练掌握价层电子对互斥理论、构造原理、元素周期律等知识点,难点是(6),同时考查学生空间想象能力、信息分析判断能力,题目难度中等.

练习册系列答案
相关题目
下列反应中属吸热反应的是( )
| A、镁与盐酸反应放出氢气 |
| B、氢氧化钠与盐酸的反应 |
| C、硫在空气或氧气中燃烧 |
| D、Ba(OH)2?8H2O晶体与NH4Cl晶体反应 |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、0.1 mol Na2O2含有的阴、阳离子总数是0.3 NA |
| B、1 mol?L-1的醋酸溶液中含醋酸分子数为NA |
| C、1.7 g 羟基(-OH)含有的电子数为0.9 NA |
| D、常温常压下,2.24 L乙烯含有的碳碳双键数为0.1 NA |
下列说法不正确的是( )
| A、海水淡化可以解决淡水供应危机,向海水中加入明矾可以使海水淡化 |
| B、我国自行研制的“神七”航天服是由新型“连续纤维增韧”材料做成的,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |
| C、“地沟油”危害健康,不仅是因为人体所必需的维生素E及脂肪酸油脂已经被破坏,营养低,而且含有黄曲霉素、苯并芘,这两种毒素都是致癌物 |
| D、纸层析法、钠熔法、铜丝燃烧法都是定性分析法 |
下列事实,不能用勒夏特列原理解释的是( )
| A、实验室用排饱和食盐水而不用排水法收集氯气 |
| B、加催化剂,使N2和H2在一定条件下转化为NH3 |
| C、N2和H2反应生成NH3,加压有利于提高 NH3的产率 |
| D、光照新制的氯水时,溶液中c(H+)增大 |
已知短周期元素的离子aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A、单质的还原性:A>B>D>C |
| B、离子半径:C>D>B>A |
| C、原子序数:d>c>b>a |
| D、原子半径:A>B>D>C |
 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.