题目内容
7.某无色溶液中大量存在以下五种离子:NO3-、SO42-、Al3+、H+、M.其物质的量之比为n(NO3-):n(SO42-):n(Al3+):n(H+):n(M)=2:3:1:3:1,则M可能为( )| A. | Cu2+ | B. | Mg2+ | C. | CO32- | D. | Na+ |
分析 无色溶液中不存在有色的Cu2+;根据各离子的物质的量之比可设n(NO3-)、n(S042-)、n(Al3+)、n(H+)、n(M)分别为2mol、3mol、1mol、3mol、1mol,然后利用电荷守恒计算出M所带电荷,从而得出M名称.
解答 解:Cu2+为有色离子,则M一定不是Cu2+;
n(NO3-):n(SO42-):n(Al3+):n(H+):n(M)=2:3:1:3:1,可设n(NO3-)、n(S042-)、n(Al3+)、n(H+)、n(M)分别为2mol、3mol、1mol、3mol、1mol,
根据电荷守恒可知:3n(Al3+)+n(H+)=6mol<n(NO3-)+2n(S042-)=8mol,故M为阳离子,且M所得电荷数为:$\frac{8mol-6mol}{1mol}$=2,说明M为带有2个正电荷的离子,选项中只有Mg2+符合,
故选B.
点评 本题考查物质的量浓度计算、离子共存问题,题目难度中等,注意根据电荷守恒判断M应为阳离子,属于易错题目,学生容易考虑电荷守恒,忽略离子共存问题,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
19.实验室用NaOH固体和蒸馏水准确配制一定物质的量浓度的NaOH溶液时,以下仪器中不需要用到的是( )
| A. | 托盘天平 | B. | 锥形瓶 | C. | 烧杯 | D. | 容量瓶 |
20.下列离子方程式的书写正确的是( )
| A. | 硫氢化钠溶液中滴入硫酸铜溶液:S2-+Cu2+═CuS↓ | |
| B. | 稀硝酸中加入过量的铁粉:Fe+6H++3NO3-═Fe3++3NO2↑+3H2O | |
| C. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| D. | 二氧化硫通入氯化铁溶液:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+ |
15.下列说法中正确的是( )
| A. | 化学反应中的能量变化都表现为热量的变化 | |
| B. | 生成物总能量一定低于反应物总能量 | |
| C. | 放热反应的反应速率总是大于吸热反应的反应速率 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同 |
2.下列物质属于电解质并能导电的是( )
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤KCl晶体 ⑥液态氯化氢.
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤KCl晶体 ⑥液态氯化氢.
| A. | ① | B. | ①⑥ | C. | ①②⑤ | D. | ①②③⑤ |
12.下列说法正确的是( )
| A. | 金属腐蚀就是金属原子失去电子被还原的过程 | |
| B. | 钢铁吸氧腐蚀时,负极的电极反应式为:2H2O+O2+4e-═4OH- | |
| C. | 在铁上镀锌时,应让锌作阴极,铁作阳极 | |
| D. | 铝制品不需要特殊的防腐措施原因是铝易于被氧气氧化形成致密的氧化物保护膜 |
16.将硝酸分解产生的气体收集于试管内然后倒立于水槽中,一段时间后试管内(假设没有空气混入)( )
| A. | 剩余NO | B. | 剩余O2 | C. | 剩余NO2 | D. | 不剩余气体 |
17.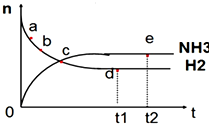 向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(NH3)和n(H2)随时间变化的关系如图所示.下列有关叙述正确的是( )
向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(NH3)和n(H2)随时间变化的关系如图所示.下列有关叙述正确的是( )
 向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(NH3)和n(H2)随时间变化的关系如图所示.下列有关叙述正确的是( )
向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(NH3)和n(H2)随时间变化的关系如图所示.下列有关叙述正确的是( )| A. | c点表示NH3生成速率与NH3分解速率相同 | |
| B. | c点和e点时反应的平衡常数相同 | |
| C. | N2的转化率:b>a | |
| D. | d点时,n(N2):n(H2):n(NH3)=1:3:2 |
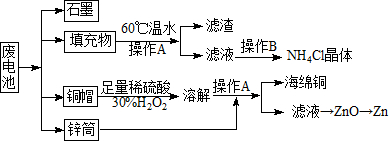 常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害.某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源
常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害.某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源