题目内容
汽车尾气净化中的一个反应如下:2NO(g)+2CO(g)?N2(g)+2CO2(g),请回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ?mol-l
C(s)+O2(g)=CO2(g)△H=-393.5 kJ?mol-l
2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-l
则2NO(g)+2CO(g)?N2(g)+2CO2(g) 的△H= kJ?mol-l.
(2)一定温度下,向体积为 1L的密闭容器中充入一定量的NO和CO.在t1时刻达到平衡状态,此时n(CO)=0.1mol,n(NO)=0.2mol,n(N2)=a mol,且N2占平衡总体积的
.
①则该反应的平衡常数K= .若保持温度及容器体积不变,平衡后在此基础上再向容器中充入3a mol的N2、0.2mol的NO,平衡将 移动(填“向左”、“向右”或“不”).
②下列各种情况,可说明该反应已经达到平衡的是 .
A.v生成(CO2)=v消耗(CO) B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变 D.NO、CO、N2、CO2的浓度均不再变化
E.单位时间内生成2n mol碳氧双键的同时消耗n molN≡N
③在t2时刻,将容器迅速压缩到原容积的
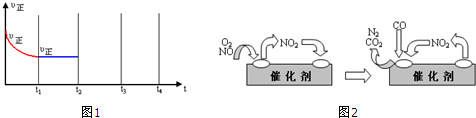
,在其它条件不变的情况下,t3时刻达到新的平衡状态.请在图1中补充画出t2-t3-t4时段,正反应速率的变化曲线:
(3)如果要净化汽车尾气的同时提高该反应的速率和NO的转化率,采取的措施是 ;
A.降低温度 B.增大压强同时加催化剂
C.升高温度同时充入N2 D.及时将CO2和N2从反应体系中移走
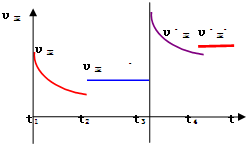
(4)为避免汽车尾气中的有害气体对大气的污染,给汽车安装尾气净化装置.净化装置里装有含Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如图2所示.
①写出上述变化中的总化学反应方程式 .
②有人提出,可以设计反应2CO(g)=2C(s)+O2(g) 来消除CO的污染.请你判断是否可行,并说出理由: .
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ?mol-l
C(s)+O2(g)=CO2(g)△H=-393.5 kJ?mol-l
2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-l
则2NO(g)+2CO(g)?N2(g)+2CO2(g) 的△H=
(2)一定温度下,向体积为 1L的密闭容器中充入一定量的NO和CO.在t1时刻达到平衡状态,此时n(CO)=0.1mol,n(NO)=0.2mol,n(N2)=a mol,且N2占平衡总体积的
| 1 |
| 4 |
①则该反应的平衡常数K=
②下列各种情况,可说明该反应已经达到平衡的是
A.v生成(CO2)=v消耗(CO) B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变 D.NO、CO、N2、CO2的浓度均不再变化
E.单位时间内生成2n mol碳氧双键的同时消耗n molN≡N
③在t2时刻,将容器迅速压缩到原容积的
| 1 |
| 2 |

(3)如果要净化汽车尾气的同时提高该反应的速率和NO的转化率,采取的措施是
A.降低温度 B.增大压强同时加催化剂
C.升高温度同时充入N2 D.及时将CO2和N2从反应体系中移走
(4)为避免汽车尾气中的有害气体对大气的污染,给汽车安装尾气净化装置.净化装置里装有含Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如图2所示.
①写出上述变化中的总化学反应方程式
②有人提出,可以设计反应2CO(g)=2C(s)+O2(g) 来消除CO的污染.请你判断是否可行,并说出理由:
考点:热化学方程式,化学平衡的影响因素,化学平衡状态的判断
专题:化学平衡专题
分析:(1)依据盖斯定律内容和含义,结合热化学方程式计算得到所需热化学方程式得到.
(2)①根据三行式结合化学平衡的移动知识来计算;
②根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
③压缩容器体积,增大了压强,正逆反应速率增大,平衡向着气体体减小的方向移动,据此画出从t2-t3-t4时段,正反应速率的变化曲线;
(3)根据影响化学反应速率的因素以及影响化学平衡移动的因素来回答;
(4)①根据已知信息书写反应物和产物并配平方程式;
②根据反应能否自发进行的判据来回答.
(2)①根据三行式结合化学平衡的移动知识来计算;
②根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
③压缩容器体积,增大了压强,正逆反应速率增大,平衡向着气体体减小的方向移动,据此画出从t2-t3-t4时段,正反应速率的变化曲线;
(3)根据影响化学反应速率的因素以及影响化学平衡移动的因素来回答;
(4)①根据已知信息书写反应物和产物并配平方程式;
②根据反应能否自发进行的判据来回答.
解答:
解:(1)已知①N2(g)+O2(g)=2NO(g)△H=+180.5kJ?mol-l
②C(s)+O2(g)=CO2(g)△H=-393.5 kJ?mol-l
③2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-l
依据盖斯定律计算②×2-①-③得到2CO(g)+2NO(g)═N2(g)+2CO2(g))△H=-746KJ/mol;
故答案为:-746.5;
(2)①2NO(g)+2CO(g)?N2(g)+2CO2(g),
平衡浓度:0.2 0.1 a 2a
则
=
,解得a=0.3
K=
=27,平衡后在此基础上再向容器中充入3amol即0.9mol的N2、0.2mol的NO,此时Qc=K,所以不移动,
故答案为:270;不;
②A.v生成(CO2)=v消耗(CO),不能证明正逆反应速率相等,故A错误;
B.混合气体的密度
,反应前后质量守恒,不变化,体积不变,所以密度始终不变,当密度不变化的状态不一定平衡,故B错误;
C.混合气体的平均相对分子质量=
,质量守恒,但是n变化,当混合气体的平均相对分子质量不再改变,达到了平衡状态,故C正确;
D.NO、CO、N2、CO2的浓度均不再变化是化学平衡的特征,故D正确.
E.单位时间内生成2n mol碳氧双键的同时消耗n molN≡N,不能证明正逆反应速率相等,故E错误.
故选CD;
③压缩容器体积,增大了压强,正逆反应速率增大,平衡向着气体体减小的方向移动,即向正方向移动,正反应速率大于逆反应速率,即
 ,故答案为:
,故答案为: ;
;
(3)A.降低温度不会加快反应速率,只能降低反应速率,故A错误;
B.增大压强同时加催化剂,能提高反应的速率和NO的转化率,故B正确;
C.升高温度能提高反应速率,但是充入N2不能提高NO的转化率,故C错误;
D.及时将CO2和N2从反应体系中移走不能提高反应速率,故D错误.
故选B.
(4)①NO2为中间产物,反应物为NO、O2、CO,产物为CO2、N2,反应方程式为2NO+O2+4CO
4CO2+N2,故答案为:2NO+O2+4CO
4CO2+N2;
②根据反应能否自发进行的判据,因为△H>0,△S<0,此时△H-T△S>0,在任何情况下都不能自发进行,故答案为:因为△H>0,△S<0,在任何情况下都不能自发进行.
②C(s)+O2(g)=CO2(g)△H=-393.5 kJ?mol-l
③2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-l
依据盖斯定律计算②×2-①-③得到2CO(g)+2NO(g)═N2(g)+2CO2(g))△H=-746KJ/mol;
故答案为:-746.5;
(2)①2NO(g)+2CO(g)?N2(g)+2CO2(g),
平衡浓度:0.2 0.1 a 2a
则
| a |
| 0.1+0.2+a+2a |
| 1 |
| 4 |
K=
| a?(2a)2 |
| 0.22?0.12 |
故答案为:270;不;
②A.v生成(CO2)=v消耗(CO),不能证明正逆反应速率相等,故A错误;
B.混合气体的密度
| m |
| V |
C.混合气体的平均相对分子质量=
| m |
| n |
D.NO、CO、N2、CO2的浓度均不再变化是化学平衡的特征,故D正确.
E.单位时间内生成2n mol碳氧双键的同时消耗n molN≡N,不能证明正逆反应速率相等,故E错误.
故选CD;
③压缩容器体积,增大了压强,正逆反应速率增大,平衡向着气体体减小的方向移动,即向正方向移动,正反应速率大于逆反应速率,即
 ,故答案为:
,故答案为: ;
;(3)A.降低温度不会加快反应速率,只能降低反应速率,故A错误;
B.增大压强同时加催化剂,能提高反应的速率和NO的转化率,故B正确;
C.升高温度能提高反应速率,但是充入N2不能提高NO的转化率,故C错误;
D.及时将CO2和N2从反应体系中移走不能提高反应速率,故D错误.
故选B.
(4)①NO2为中间产物,反应物为NO、O2、CO,产物为CO2、N2,反应方程式为2NO+O2+4CO
| ||
| ||
②根据反应能否自发进行的判据,因为△H>0,△S<0,此时△H-T△S>0,在任何情况下都不能自发进行,故答案为:因为△H>0,△S<0,在任何情况下都不能自发进行.
点评:本题涉及热化学盖斯定律的应用、化学平衡的有关计算、化学平衡状态的判断等方面的知识,属于综合知识的考查题,难度大.

练习册系列答案
相关题目
下列各组物质中最简式相同,但既不是同系物又不是同分异构体的是( )
| A、丙烯和环丙烷 |
| B、甲醛和乙酸 |
| C、乙酸和甲酸甲酯 |
| D、乙醛和乙酸乙酯 |
下列物物质中,可证明某晶体是离子晶体的是( )
| A、易溶于水 |
| B、晶体不导电,熔化时能导电 |
| C、熔点较高 |
| D、晶体不导电,水溶液能导电 |