题目内容
15.下列混合物的分离方法不可行的是( )| A. | 互溶的液态混合物可用分液的方法分离 | |
| B. | 互不相溶的液态混合物可用分液的方法分离 | |
| C. | 沸点不同的液态混合物可用蒸馏的方法分离 | |
| D. | 氯化钠和氧化铜形成的混合物可以按溶解、过滤、蒸发的顺序分离 |
分析 A.互溶的液态混合物,利用沸点差异分离;
B.互不相溶的液态混合物,分层;
C.沸点不同的液态混合物,可利用蒸馏分离;
D.CuO不溶于水,NaCl溶于水.
解答 解:A.互溶的液态混合物,利用沸点差异分离,则选蒸馏法分离,故A错误;
B.互不相溶的液态混合物,分层,则选择分液法分离,故B正确;
C.沸点不同的液态混合物,可利用蒸馏分离,故C正确;
D.CuO不溶于水,NaCl溶于水,则溶解、过滤、蒸发的顺序分离,故D正确;
故选A.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意分离原理,题目难度不大.

练习册系列答案
相关题目
5.下表是元素周期表的一部分.
根据A~H元素在周期表中的位置,用化学式填写空白.
(1)氧化性最强的单质是F2,还原性最强的单质是Na,化学性质最不活泼的单质是Ne.(填相应的化学式)
(2)最稳定的氢化物是HF.(填相应的化学式)
(3)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是NaOH、Al(OH)3、H3PO4、HClO4.(填相应的化学式)
(4)一个E原子的核外电子总共有15种运动状态.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | F | H | |||||
| 3 | B | C | E | G |
(1)氧化性最强的单质是F2,还原性最强的单质是Na,化学性质最不活泼的单质是Ne.(填相应的化学式)
(2)最稳定的氢化物是HF.(填相应的化学式)
(3)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是NaOH、Al(OH)3、H3PO4、HClO4.(填相应的化学式)
(4)一个E原子的核外电子总共有15种运动状态.
6.在一个氧化还原反应的体系中,共有SO2、O2、Fe2O3、FeS2四种物质.在反应中测得O2和Fe2O3的物质的量随时间变化如图所示.下列有关判断中正确的是( )

| A. | O2中只存在非极性共价键,SO2是共价化合物 | |
| B. | 氧化剂是O2,还原产物只有Fe2O3 | |
| C. | 每消耗22.4LO2,即转移4NA个电子 | |
| D. | SO2溶于水之后的溶液可以导电,所以SO2是电解质 |
10.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,2.24LH2O中分子的数目为0.1NA | |
| B. | 0.1mol•L-1NH4Cl溶液中含有Cl-的数目为0.1NA | |
| C. | 常温下,1.7gNH3中含有氢原子数目为0.3 NA | |
| D. | 5.6g铁粉在足量的氯气中充分燃烧,转移电子数为0.2NA |
20.为测定某血液样品中钙离子的含量,可取该样品2.00mL用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀.将沉淀用稀硫酸处理得H2C2O4后,再用1.000×10-4mol•L-1酸性KMnO4标准溶液滴定,到达终点时用去20.00mL标准液.则下列说法中错误的是( )
| A. | 用酸性KMnO4(aq)滴定H2C2O4(aq)的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O | |
| B. | KMnO4标准溶液应用式碱滴定管盛装 | |
| C. | 滴定终点时的现象为:最后1滴标准KMnO4(aq)使锥形瓶中溶液由无色变为浅紫色,且约半分钟内不褪色 | |
| D. | 经计算该样品中钙离子浓度为1.000×10-4g•mL-1 |
7.pmolC2H4在密闭容器中加强热分解,达到平衡时生成mmolC2H2和nmolH2,将平衡混合气体完全燃烧生成水和二氧化碳,要消耗氧气( )
| A. | ($\frac{3m}{2}$+$\frac{n}{2}$+2p)mol | B. | (3p-$\frac{3m}{2}$-$\frac{n}{2}$)mol | C. | 3pmol | D. | ($\frac{3m}{2}$+$\frac{n}{2}$)mol |
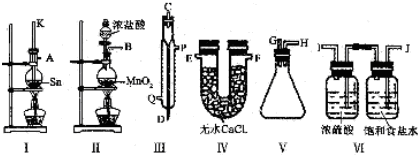
4.实验室用浓硫酸和乙醇反应制备乙烯,若温度过高或加热时间过长,制得的乙稀往往混有CO2、SO2、H2O(气体少量).请回答下列问题:
(1)试分析CO2和SO2 是怎么样产生的?乙醇或乙烯与浓硫酸发生氧化还原反应生成CO2和SO2(用一句话说明).
(2)试用如图所示的装置设计一个实验,验证制得的气体中确实含有CO2和SO2、H2O(g),按气流的方向,各装置的连接顺序是:④②①③.
(3)实验时若观察到:①中A瓶中溶液褪色,B瓶中溶液颜色逐渐变浅,C瓶中溶液不褪色,则C瓶的作用是检验SO2是否除尽.
(4)装置②中所加的试剂名称是无水硫酸铜,简述确定装置②在整套装置中的位置的理由是①③导出的气体带有水蒸气,影响水蒸气的确定.
(1)试分析CO2和SO2 是怎么样产生的?乙醇或乙烯与浓硫酸发生氧化还原反应生成CO2和SO2(用一句话说明).
(2)试用如图所示的装置设计一个实验,验证制得的气体中确实含有CO2和SO2、H2O(g),按气流的方向,各装置的连接顺序是:④②①③.
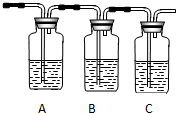 品红溶液 KMnO4 溶液品红溶液 品红溶液 KMnO4 溶液品红溶液 ① |  ② ② | 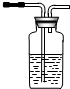 ③ | 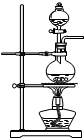 ④ |
(4)装置②中所加的试剂名称是无水硫酸铜,简述确定装置②在整套装置中的位置的理由是①③导出的气体带有水蒸气,影响水蒸气的确定.

 利用CH4和CO2可以制造价值更高的化学产品.已知下列反应:
利用CH4和CO2可以制造价值更高的化学产品.已知下列反应: