题目内容
将过量的CO2分别通入①CaCl2溶液;②Na2SiO3溶液;③NaAlO2溶液;④饱和Na2CO3溶液;⑤Ca(OH)2.最终溶液中有白色沉淀析出的是( )
| A、①②③④⑤ | B、②③④ |
| C、②④⑤ | D、①②④ |
考点:钠的重要化合物
专题:
分析:①化学反应的原则是:酸性强的酸制弱酸弱的酸,一般情况不能由弱酸制强酸.碳酸的酸性强于硅酸、次氯酸,弱于盐酸;
②硅酸钠溶液通二氧化碳,生成硅酸和碳酸钠,硅酸是不溶于水的沉淀;
③NaAlO2溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠;
④饱和Na2CO3溶液通入足量的二氧化碳,生成碳酸氢钠,碳酸氢钠溶解度小于碳酸钠,沉淀析出;
⑤澄清石灰石中通入足量的二氧化碳生成可溶性的碳酸氢钙可溶性溶液,不会产生沉淀.
②硅酸钠溶液通二氧化碳,生成硅酸和碳酸钠,硅酸是不溶于水的沉淀;
③NaAlO2溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠;
④饱和Na2CO3溶液通入足量的二氧化碳,生成碳酸氢钠,碳酸氢钠溶解度小于碳酸钠,沉淀析出;
⑤澄清石灰石中通入足量的二氧化碳生成可溶性的碳酸氢钙可溶性溶液,不会产生沉淀.
解答:
解:①CaCl2溶液与二氧化碳不反应,故①不会产生沉淀;
②硅酸钠溶液通二氧化碳反应:Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3硅酸是一种白色沉淀,故②产生白色沉淀;
③NaAlO2溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠,2H2O+NaAlO2+CO2=Al(OH)3↓+NaHCO3,故③产生白色沉淀;
④饱和Na2CO3溶液通入足量的二氧化碳,由Na2CO3+H2O+CO2=2NaHCO3可知,此反应消耗水,且Na2CO3转化为NaHCO3后溶质质量增加,又因NaHCO3溶解度较小,所以会有晶体析出,故④会产生沉淀,
⑤Ca(OH)2通入过量的二氧化碳,2CO2+Ca(OH)2=Ca(HCO3)2,不会产生沉淀,故⑤不会产生沉淀;
故选B.
②硅酸钠溶液通二氧化碳反应:Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3硅酸是一种白色沉淀,故②产生白色沉淀;
③NaAlO2溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠,2H2O+NaAlO2+CO2=Al(OH)3↓+NaHCO3,故③产生白色沉淀;
④饱和Na2CO3溶液通入足量的二氧化碳,由Na2CO3+H2O+CO2=2NaHCO3可知,此反应消耗水,且Na2CO3转化为NaHCO3后溶质质量增加,又因NaHCO3溶解度较小,所以会有晶体析出,故④会产生沉淀,
⑤Ca(OH)2通入过量的二氧化碳,2CO2+Ca(OH)2=Ca(HCO3)2,不会产生沉淀,故⑤不会产生沉淀;
故选B.
点评:本题考查了碳的氧化物及其对应碳酸盐和碳酸氢盐的性质,题目难度不大,注意碳酸钠和碳酸氢钠溶解性的差别.

练习册系列答案
相关题目
关于糖类、脂肪和蛋白质,以下叙述正确的是( )
| A、植物油不能使溴的四氯化碳溶液褪色 |
| B、葡萄糖能发生氧化反应和水解反应 |
| C、淀粉水解的最终产物是葡萄糖 |
| D、蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
化学与生产、生活、社会密切相关.下列说法中正确的是( )
| A、合金材料中可能含有非金属元素 |
| B、铁在潮湿的空气中放置,易发生化学腐蚀而生锈 |
| C、二氧化硫和氯水均具有漂白性,可将两者混合使用增强漂白效果 |
| D、氮化硅陶瓷、光导纤维、石英玻璃都属于新型无机非金属材料 |
已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB-?H++B2-,则下列说法中一定正确的是( )
| A、NaHB溶液一定呈酸性,Na2B溶液一定呈碱性 |
| B、Na2B溶液一定呈碱性,NaHB溶液可能呈酸性也可能呈碱性 |
| C、NaHB水溶液中一定有:c(Na+)+c(H+)=c(HB-)+c(OH-)+c(B2-) |
| D、在Na2B溶液中一定有:c(OH-)=c(H+)+c(HB-) |
在密闭容器中,反应A(g)+B(g)?C(g)达到平衡后,若增大A的浓度或增大压强使平衡向右移动.下列说法中正确的是( )
| A、C的百分含量一定增大 |
| B、C的浓度一定增大 |
| C、A的百分含量一定增大 |
| D、A的转化率一定增大 |
同温同压下,等质量的下列气体体积最小的是( )
| A、氢气 | B、氯气 |
| C、氧气 | D、氯化氢. |
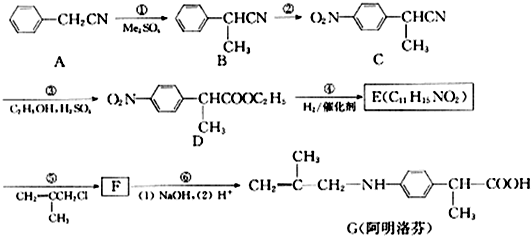
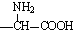 ②含有对位二取代苯环
②含有对位二取代苯环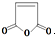 是合成某些药物的中间体.试设计合理方案由化合物
是合成某些药物的中间体.试设计合理方案由化合物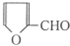 合成
合成 .
. 在400℃有金属氧化物存在条件下能发生脱羰基(
在400℃有金属氧化物存在条件下能发生脱羰基(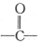 )反应.
)反应.
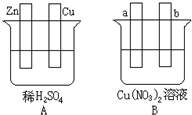 按要求对如图中两极进行必要的联接并填空,a、b为惰性材料.
按要求对如图中两极进行必要的联接并填空,a、b为惰性材料.