题目内容
CH3COONa稀溶液中分别加入少量下列物质或改变如下条件,能使比值
一定减小的是( )
①固体NaOH ②固体KOH ③固体NaHSO4④固体CH3COONa ⑤冰醋酸 ⑥降温.
| c(CH3COO-) |
| c(Na+) |
①固体NaOH ②固体KOH ③固体NaHSO4④固体CH3COONa ⑤冰醋酸 ⑥降温.
| A、只有①③ | B、①③④ |
| C、②④⑤⑥ | D、③④⑥ |
考点:影响盐类水解程度的主要因素
专题:
分析:醋酸钠溶液中存在醋酸根离子水解平衡:CH3COO-+H2O?CH3COOH+OH-,使
比值减小,可使平衡向正反应方向移动,结合影响水解平衡移动的因素解答该题.
| c(CH3COO-) |
| c(Na+) |
解答:
解:①加入固体NaOH,c(Na+)与c(CH3COO-)都增大,但c(Na+)增大幅度较大,则
比值减小,故①符合;
②加入固体KOH,抑制水解,则c(CH3COO-)增大,而c(Na+)不变,则
比值增大,故②不符合;
③加入固体NaHSO4,平衡向正向移动,c(Na+)增大,c(CH3COO-)减小,则
比值减小,故③符合;
④加入固体CH3COONa,浓度增大,水解程度降低,则
比值增大,故④不符合;
⑤加入冰醋酸,c(CH3COO-)增大,则
比值增大,故⑤不符合.
⑥水解平衡时吸热反应,降温,平衡逆向进行,醋酸根离子浓度增大,则
比值增大,故⑥不符合.
故选A.
| c(CH3COO-) |
| c(Na+) |
②加入固体KOH,抑制水解,则c(CH3COO-)增大,而c(Na+)不变,则
| c(CH3COO-) |
| c(Na+) |
③加入固体NaHSO4,平衡向正向移动,c(Na+)增大,c(CH3COO-)减小,则
| c(CH3COO-) |
| c(Na+) |
④加入固体CH3COONa,浓度增大,水解程度降低,则
| c(CH3COO-) |
| c(Na+) |
⑤加入冰醋酸,c(CH3COO-)增大,则
| c(CH3COO-) |
| c(Na+) |
⑥水解平衡时吸热反应,降温,平衡逆向进行,醋酸根离子浓度增大,则
| c(CH3COO-) |
| c(Na+) |
故选A.
点评:本题考查学生盐的水解原理以及影响盐的水解平衡移动等方面的知识,为高频考点,侧重于学生的分析能力的考查,注意知识的归纳整理是解题关键,难度中等.

练习册系列答案
相关题目
有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现出不同的性质.下列现象不能说明上述观点的是( )
| A、甲苯能使酸性KMnO4溶液褪色,而甲基环己烷不能使酸性KMnO4溶液褪色 |
| B、乙烯能与溴水发生加成反应,而乙烷不能与溴水发生加成反应 |
| C、苯酚与溴水可以直接反应,而苯与液溴反应则需要铁作催化剂 |
| D、苯酚可以与NaOH反应,而乙醇不能与NaOH反应 |
下列各个装置中能组成原电池的是( )
A、 稀硫酸 |
B、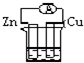 CuSO4 |
C、 酒精溶液 |
D、 稀硫酸 稀硫酸 |
在铁的吸氧腐蚀中,发生还原反应的电极上进行的电极反应是( )
| A、2 H++2e-═H2↑ |
| B、O2+2H2O+4e-═4OH- |
| C、Fe-2e-═Fe2+ |
| D、4 OH--4e-═2H2O+O2↑ |
下列各组元素中按微粒半径递增顺序排列的是( )
| A、Li K Na |
| B、Ba2+ Ca2+ Mg2+ |
| C、Ca2+ K+ Cl- |
| D、N O F |
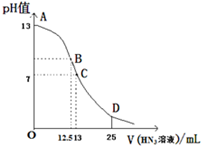 纯叠氮酸(HN3)是无色液体,对热十分稳定,但受撞击就爆炸,常用作引爆剂,如图为常温下向25ml0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1的HN3溶液过程中溶液的pH的变化曲线(溶液混合时体积变化忽略不计).
纯叠氮酸(HN3)是无色液体,对热十分稳定,但受撞击就爆炸,常用作引爆剂,如图为常温下向25ml0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1的HN3溶液过程中溶液的pH的变化曲线(溶液混合时体积变化忽略不计).