题目内容
17.已知化学方程式中各物质的化学计量数之比等于同温同压下气体的体积之比.在常温常压下,H2和O2的混合气体为aL,用电火花引燃后恢复室温,剩余气体的体积为bL,求原混合气体中H2和O2的体积之比.分析 氢气和氧气反应的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,最后剩余bL气体,则反应消耗了(a-b)L气体,根据反应方程式计算出反应消耗的氧气和氢气的体积,再结合剩余的气体可能为氢气或氧气计算出原混合气体中氢气和氧气的体积.
解答 解:氢气和氧气的反应方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,反应消耗的气体总体积为:aL-bL=(a-b)L,
该温度下水为液体,参加反应的氢气体积为:$\frac{2}{3}$(a-b)L,参加反应的氧气体积为:$\frac{1}{3}$(a-b)L,
当剩余气体为氢气时,原混合气体中氢气总体积为:$\frac{2}{3}$(a-b)L+bL=$\frac{1}{3}$(2a+b)L,混合气体中O2的体积氧气体积为:$\frac{1}{3}$(a-b)L,此时混合气体中H2和O2的体积之比为:$\frac{2a+b}{a-b}$;
当剩余气体为氧气时,原混合气体中氢气总体积为:$\frac{2}{3}$(a-b)L,混合气体中O2的体积氧气体积为:$\frac{1}{3}$(a-b)L+bL=$\frac{1}{3}$(a+2b)L,此时混合气体中H2和O2的体积之比为:$\frac{2(a-b)}{a+2b}$,答:当剩余气体为氢气时,原混合气体中H2和O2的体积之比为$\frac{2a+b}{a-b}$;当剩余气体为氧气时,原混合气体中H2和O2的体积之比为$\frac{2(a-b)}{a+2b}$.
点评 本题考查混合物反应的计算,题目难度中等,明确发生反应实质为解答关键,注意掌握讨论法在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.

| A. | Fe2+、Cl-、Na+、NO3- | B. | K+ Na+、NO3-、HCO3- | ||
| C. | Na+、Ba2+、Cl-、NO3- | D. | Na+、K+、[Al(OH)4]-、SO42- |
| A. | H2SiO3 | B. | H3PO4 | C. | H2SO4 | D. | HClO |
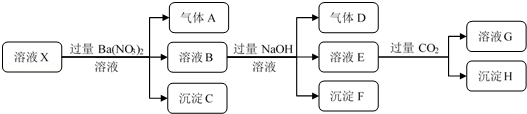
| A. | 根据上述连续实验不能确定溶液X中是否含有Fe3+ | |
| B. | 沉淀H为Al(OH)3 | |
| C. | 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- | |
| D. | 若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.15 mol•L |
| 选项 | 操作及现象 | 结论 |
| A | 取少量溶液于试管中,滴加BaCl2溶液,有白色沉淀生成,加稀硝酸沉淀不溶解 | 溶液中含有Ag+或SO42- |
| B | 取少量溶液于试管中,滴加新制氯水,溶液由无色变为黄色 | 溶液中含有Br- |
| C | 取少量溶液于试管中,滴加浓氢氧化钠溶液,微热,试管口湿润的红色石蕊试纸变蓝 | 溶液中含有NH4+ |
| D | 取少量溶液于试管中,滴加新制氯水后再滴加KSCN溶液,溶液变红色 | 原溶液中含有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
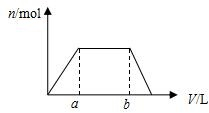 将足量CO2通入100mLKOH和Ca(OH)2的混合溶液中,生成沉淀的物质的量(n)和通入标况下CO2体积(V)的关系如图所示,则混合溶液中KOH的物质的量浓度为( )
将足量CO2通入100mLKOH和Ca(OH)2的混合溶液中,生成沉淀的物质的量(n)和通入标况下CO2体积(V)的关系如图所示,则混合溶液中KOH的物质的量浓度为( )| A. | 10(b-a)/22.4 mol/L | B. | 20(b-a)/22.4 mol/L | ||
| C. | 10b/22.4 mol/L | D. | 10a/22.4 mol/L |
| A. | 煤可以直接液化,使煤与氢气作用生成液体燃料 | |
| B. | 利用风能、生物能发电,将火力发电用煤进行脱硫处理,有利于环保 | |
| C. | 氮化硅陶瓷、通讯光缆等都是新型无机非金属材料 | |
| D. | 塑料、橡胶、纤维这三大材料都是以石油、煤、天然气为原料生产的 |