题目内容
6.化字与日常生活密切相关,下列说法错误的是( )| A. | 单质硅是将太阳能转化为电能的常用材料 | |
| B. | 服用铬含量超标的药用胶囊会对人体健康造成危害 | |
| C. | 氢氧化铝可作胃酸的中和剂 | |
| D. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
分析 A.单质硅可以制太阳能电池板;
B.一些重金属离子(如Cu2+、Ba2+、Pb2+、Ag+等)与蛋白质作用会使蛋白质变性而丧失其生理功能;
C.氢氧化铝为难溶物,能够中和胃酸中的盐酸;
D.明矾溶于水发生水解反应,生成氢氧化铝胶体,氢氧化铝胶体可以吸附杂质.
解答 解:A.单质硅可以制太阳能电池板,是将太阳能转化为电能,故A正确;
B.重金属铬能与蛋白质发生作用,使其丧失生理活性,对人体造成危害,故B正确;
C.氢氧化铝能够与胃酸中的盐酸反应,能够作胃酸的中和剂,故C正确;
D.明矾[KAl(SO4)2•12H2O]作为净水剂是因为明矾溶于水发生水解反应,反应的离子方程式为:Al3++3H2O?Al(OH)3+3H+,生成氢氧化铝胶体,氢氧化铝胶体可以吸附杂质,不能作漂白剂,故D错误.
故选D.
点评 本题考查了生活中常见物质的性质及用途,注意知识的迁移和应用在解题中的应用是解题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | pH相同的①CH3COONa ②NaHCO3 ③NaClO三种溶液的c(Na+):③>②>① | |
| B. | 0.2mol•L-1 CH3COOH溶液与0.1mol•L-1NaOH溶液等体积混合2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) | |
| C. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O═2HClO+CO32- | |
| D. | 常温下,向0.1mol/L NH4HSO4溶液中滴加NaOH溶液至中性c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
18.四种短周期元素在周期表中的相对位置如下所示,其中Z元素最外层电子数是其电子层数的2倍.下列说法正确的是( )
| X | Y | |
| Z | W |
| A. | 四种短周期元素中W的原子半径最小 | |
| B. | Z元素在周期表中的位置是第三周期第ⅣA族 | |
| C. | 原子最外层电子数由多到少的顺序:Y>X>W>Z,最高正价由高到低顺序:W>Z | |
| D. | 元素非金属性由强到弱的顺序:W>Z,W的单质常温下可与氢氧化钠溶液反应 |
1.下列离子在溶液中能大量共存的是( )
| A. | Cu2+ Na+ NO3- S2- | B. | Mg2+ H+ SO42- NO3- | ||
| C. | Al3+ Na+ HCO3- SO42- | D. | Fe3+ H+ SCN- Cl- |
1.已知氧化性Br2>Fe3+.FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为:a Fe2++b Br-+c Cl2→d Fe3++e Br2+f Cl-下列选项中的数字与离子方程式中的a.b.c.d.e.f一一对应,其中不符合反应实际的是( )
| A. | 2 4 3 2 2 6 | B. | 0 2 1 0 1 2 | ||
| C. | 2 0 1 2 0 2 | D. | 2 2 2 2 1 4 |
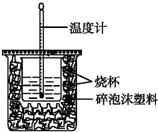 (1)已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
(1)已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: