题目内容
3.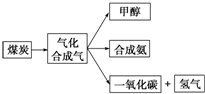 (1)如图是某煤化工产业链的一部分:
(1)如图是某煤化工产业链的一部分:已知该产业链中某反应的平衡常数表达式为K=$\frac{c({H}_{2})•c(CO)}{c({H}_{2}O)}$,已知此反应中生成1g氢气需吸热65.75KJ,它所对应反应的热化学方程式是C(s)+H2O(g)?CO(g)+H2(g)△H=+131.5KJ/mol
(2)向2L密闭容器中加入2mol CO2、6mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)
①该反应自发进行的条件是低温(填“低温”、“高温”或“任意温度”)
②下列叙述能说明容器内反应达到平衡状态的是D.
A.混合气体的平均相对分子质量保持不变 B.CO2和H2的体积分数保持不变
C.CO2和H2的转化率相等 D.混合气体的密度保持不变.
分析 (1)产业链中某反应的平衡常数表达式为K=$\frac{c({H}_{2})•c(CO)}{c({H}_{2}O)}$,反应的化学方程式为:H2O(g)+C(s)?H2(g)+CO(g),已知此反应中生成1g氢气需吸热65.75KJ,生成2g氢气放热=65.75KJ×2=131.5KJ,结合热化学方程式书写方法写出,标注物质聚集状态和对应反应的焓变;
(2)①自发进行的判断依据是△H-T△S<0,结合反应特征分析判断需要的条件;
②可能反应到达平衡时,正逆反应速率相等,各组分的浓度、含量不变,由此衍生的其它一些物理量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不变化,说明到达平衡.
解答 解:(1)产业链中某反应的平衡常数表达式为K=$\frac{c({H}_{2})•c(CO)}{c({H}_{2}O)}$,反应是碳和水蒸气反应生成氢气和一氧化碳,反应的化学方程式为:H2O(g)+C(s)?H2(g)+CO(g),已知此反应中生成1g氢气需吸热65.75KJ,生成2g氢气放热=65.75KJ×2=131.5KJ,结合热化学方程式书写方法写出,标注物质聚集状态和对应反应的焓变,反应的热化学方程式为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.5 KJ/mol,
故答案为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.5 KJ/mol;
(2)①CO2(g)+3H2(g)═CH3OH(l)+H2O(l),熵变△S<0,则反应焓变△H<0,低温下满足△H-T△S<0,
故答案为:低温;
②CO2(g)+3H2(g)═CH3OH(l)+H2O(l),
A、向2L密闭容器中加入2mol CO2、6mol H2,按照1:3反应,所以混合气体的平均相对分子质量始终保持不变,不能说明反应达到平衡状态,故A错误;
B、向2L密闭容器中加入2mol CO2、6mol H2,按照1:3反应,所以过程中CO2和H2的体积分数始终保持不变,故B错误;
C、向2L密闭容器中加入2mol CO2、6mol H2,按照1:3反应,CO2和H2的转化率始终相等,不能确定反应是否达到平衡状态,故C错误;
D、反应物是气体,生成物是液体,混合气体的密度保持不变,说明反应达到平衡状态,故D正确;
故答案为:D.
点评 本题考查了化学反应原理的分析,反应化学方程式和平衡常数的关系,热化学方程式书写方法和反应自发性的判断、化学平衡状态判断,难度中等,注意基础知识的积累.

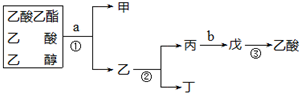
| A. | 甲是乙酸乙酯 | |
| B. | ①、②操作都是蒸馏 | |
| C. | a试剂是饱和Na2CO3溶液 | |
| D. | 制备乙酸乙酯时加试剂的顺序是:乙醇、浓硫酸、乙酸 |
| A. | x=4 | B. | 平衡向正反应方向移动 | ||
| C. | B的转化率降低 | D. | C的体积分数增大 |
| A. | 不变、减小 | B. | 增大、减小 | C. | 减小、增大 | D. | 不变、增大 |
| A. | 除去粗盐中不溶性杂质的操作有溶解、过滤、蒸发 | |
| B. | 教材上铝热反应实验中KClO3的作用是使镁带剧烈燃烧 | |
| C. | 石蜡油蒸气在炽热碎瓷片的作用下分解产生的气体可使酸性高锰酸钾溶液褪色 | |
| D. | 除去乙醇中少量的水采用加入新制的Ca(OH)2再蒸馏的方法 |
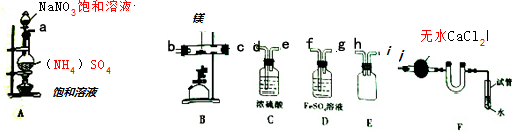
(1)装置A中反应的化学方程式为2NaNO2+(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O.
(2)按气流方向的连接顺序是(填入仪器接口字母编号):a→( h )( i )→( f )( g )→( d )( e )→( b ) ( c )→j.
(3)装置E的作用是作安全瓶,防倒吸.
(4)能否将C与D的位置对调并说明理由否,对调后不能除去水蒸气
(5)反应过程中,装置F中的末端导管必须始终插入水中,目的是防止反应过程中空气进入硬质玻璃管
(6)请用化学方法确定是否有氮化镁生成,写出实验操作及现象取少量产物于试管中,加适量蒸馏水溶解,将湿润的红色石蕊试纸放在试管口,若试纸变蓝,证明有氮化镁生成
(7)数据记录如下:
| 空硬质玻璃管质量 | 硬质玻璃管与镁的质量 | 硬质玻璃管与产物的质量 |
| 142.312g | 142.480g | 142.550g |
②若没有装置D,请比较x与3的大小,并给出判断依据x<3,若没有装置D,氮气中混有氧气,产物中混有MgO,等质量的Mg分别与O2、N2反应时,生成MgO的质量大于Mg3N2,导致计算样品中N元素质量偏大,故因此$\frac{n(Mg)}{n(O)}$<$\frac{3}{2}$,即x<3.
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
 .
.