题目内容
10.已知25℃时BaSO4的溶度积Ksp=1.1×10-10.求其溶解度常数.分析 根据BaSO4溶液中存在的沉淀溶解平衡BaSO4(s)?Ba2+(aq)+SO42-(aq)可知,Ksp(BaSO4)=c(Ba2+)•(SO42-),且c(Ba2+)=(SO42-),据此可计算出溶液中溶解的硫酸钡的物质的量浓度,再根据S=$\frac{溶质的质量}{溶剂的质量}$×100g计算;
解答 解:根据BaSO4溶液中存在的沉淀溶解平衡BaSO4(s)?Ba2+(aq)+SO42-(aq)可知,Ksp(BaSO4)=c(Ba2+)•(SO42-),且c(Ba2+)=(SO42-),所以溶液中c(BaSO4)=(SO42-)=$\sqrt{{K}_{sp}{\;}_{(BaS{O}_{4)}}}$=1.05×10-5mol•L-1,设溶液的体积为1L,则溶液中水的质量约为1000g,所含有硫酸钡的物质的量为1.05×10-5mol,所以硫酸钡的溶解度=$\frac{1.05×1{0}^{-5}×233}{1000}$×100g=2.44×10-4g,
答:25℃时BaSO4的溶解度为2.44×10-4g.
点评 本题考查了难溶电解质的溶解平衡常数与溶解度的相关计算,难度不大,注意根据溶度积常数计算离子浓度,再利用溶解度公式计算;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.25℃时,在饱和氯水中存在平衡:Cl2+H2O═H++Cl-+HClO.下列叙述中错误的是( )
| A. | 在饱和氯水中通入H2S气体,溶液的pH变小 | |
| B. | 在饱和氯水中通入SO2气体,溶液的pH变小 | |
| C. | 在饱和氯水中加入CaCO3,平衡向右移,溶液的pH变大 | |
| D. | 在饱和氯水中加入NaOH使pH=7,所得溶液中微粒浓度:c(Na+)>c(ClO-)>c(Cl-)>c(HClO) |
5.在标准状况下,下列物质占体积最大的是( )
| A. | 98g H2SO4 | B. | 6.02×1023个氮分子 | ||
| C. | 44.8L HCl | D. | 6g氢气 |
17.将分别通入下列种溶液中,有关说法正确的是( )
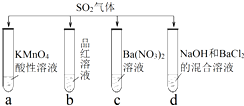

| A. | 试管a中实验可以证明具有漂白性 | |
| B. | 试管b中溶液褪色,说明具有强氧化性 | |
| C. | 试管c中能产生白色沉淀,说明具有还原性 | |
| D. | 试管d中能产生白色沉淀,该沉淀完全溶于 稀硝酸 |
 Al(OH)3+3H+,生成的胶体能吸附水中的悬浮物,从而达到净水目的.
Al(OH)3+3H+,生成的胶体能吸附水中的悬浮物,从而达到净水目的.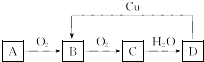
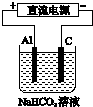 某蓄电池的反应为NiO2+Fe+2H2O$?_{放电}^{充电}$Fe(OH)2+Ni(OH)2.
某蓄电池的反应为NiO2+Fe+2H2O$?_{放电}^{充电}$Fe(OH)2+Ni(OH)2.