题目内容
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol Fe与足量的稀硝酸反应,转移3nA个电子 |
| B、常温下,16g CH4含有8nA个电子(相对原子质量:C-12,H-1) |
| C、0.5 mol?L-1Na2CO3溶液中含有nA个Na+ |
| D、标准状况下,22.4L氯水含有nA个Cl2分子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、铁与足量稀硝酸反应变为+3价;
B、求出甲烷的物质的量,然后根据1mol甲烷含10mol电子来分析;
C、溶液体积不明确;
D、氯水是氯气的水溶液.
B、求出甲烷的物质的量,然后根据1mol甲烷含10mol电子来分析;
C、溶液体积不明确;
D、氯水是氯气的水溶液.
解答:
解:A、铁与足量稀硝酸反应变为+3价,故1mol铁转移3mol电子,故A正确;
B、16g甲烷的物质的量为1mol,而1mol甲烷含10mol电子,故B错误;
C、溶液体积不明确,故无法计算溶液中的钠离子的个数,故C错误;
D、氯水为氯气的水溶液,是混合物,其中的氯气分子的个数无法计算,故D错误.
故选A.
B、16g甲烷的物质的量为1mol,而1mol甲烷含10mol电子,故B错误;
C、溶液体积不明确,故无法计算溶液中的钠离子的个数,故C错误;
D、氯水为氯气的水溶液,是混合物,其中的氯气分子的个数无法计算,故D错误.
故选A.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验事实不能用平衡移动原理解释的是( )
A、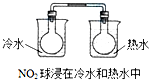 | ||||||||
B、
| ||||||||
C、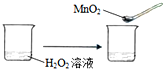 | ||||||||
D、
|
设NA表示阿伏加德罗常数的值,下列表述不正确的是( )
| A、标准状况下,22.4L氢气所含原子数是2NA |
| B、5.4g水所含的分子数为0.3NA |
| C、1mol金属钠与水反应失去的电子数为NA |
| D、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
设NA为阿伏伽德罗常数的数值.下列说法正确的是( )
| A、1mol?L-1的NaClO溶液中含有Na+的数目为NA |
| B、标准状况下,6.72LSO3中,含有硫原子的数目为0.3NA |
| C、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
| D、标准状况下,6.72LNO2与水充分反应转移的电子数目为0.1NA |
下列各组离子,在强酸性溶液中可以大量共存的是( )
| A、K+、Na+、NO3-、SiO32- |
| B、K+、Na+、Ba2+、SO42- |
| C、K+、Ca2+、Na+、CO32- |
| D、H+、NH4+、K+、Cl- |
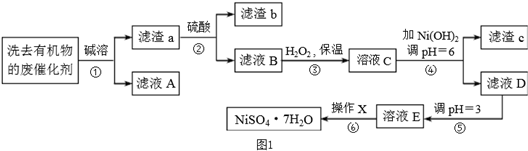

 ,其工业合成路线如下:
,其工业合成路线如下:

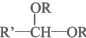 +H2O在横线上填入物质、在方框内填上系数完成聚乙烯醇转化为维纶的化学方程式.
+H2O在横线上填入物质、在方框内填上系数完成聚乙烯醇转化为维纶的化学方程式.