题目内容
(7分) 研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)这三种氧化物中,属于酸性氧化物的是____________(用化学式表示)。
(2)NO2可用水吸收,相应的化学反应方程式为 。利用反应6NO2+8NH  7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
(3)已知:2SO2(g)+O2(g) 2SO3(g) ΔH1= - 196.6 kJ·mol-1
2SO3(g) ΔH1= - 196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH2= - 113.0 kJ·mol-1
2NO2(g) ΔH2= - 113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的 ΔH3= kJ·mol-1。
SO3(g)+NO(g)的 ΔH3= kJ·mol-1。
(共7分)
(1)SO2(1分)
(2)3NO2+H2O=2HNO3+NO (2分) 6.72L (2分)
(3)—41.8 (2分)
【解析】
试题分析:(1)能与碱反应生成盐和水的氧化物是酸性氧化物,这三种氧化物中,只有SO2属于酸性氧化物。
(2)NO2与H2O反应生成HNO3和NO,化学方程式为:3NO2+H2O=2HNO3+NO;反应6NO2+8NH3 7N2+12H2O中,6NO2中N元素化合价降低,由+4价降低到0价,则6molNO2参加反应,转移24mol电子,所以当转移1.2mol电子时,消耗NO20.3mol,标准状况下体积为6.72L。
7N2+12H2O中,6NO2中N元素化合价降低,由+4价降低到0价,则6molNO2参加反应,转移24mol电子,所以当转移1.2mol电子时,消耗NO20.3mol,标准状况下体积为6.72L。
(3)已知:①2SO2(g)+O2(g)?2SO3(g)△H1= -196.6kJ?mol-1
②2NO(g)+O2(g)?2NO2(g)△H2= -113.0kJ?mol-1,利用盖斯定律将①×1/2-②×1/2得NO2(g)+SO2(g)?SO3(g)+NO(g)△H3=1/2×(-196.6kJ?mol-1)- 1/2×(-113.0kJ?mol-1)= -41.8kJ?mol-1。
考点:本题考查酸性氧化物的判断、化学方程式的书写、氧化还原反应的计算、热化学方程式的书写。

 阅读快车系列答案
阅读快车系列答案根据表中信息判断,下列选项不正确的是
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO4- | Cl2、Mn2+ |
A.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
B.第①组反应的氧化产物为O2
C.第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2
D.第③组反应中生成1mol Cl2,转移电子2mol
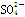 +Ba2++2OH-===BaSO4↓+Fe(OH)2↓
+Ba2++2OH-===BaSO4↓+Fe(OH)2↓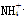 +Fe3++
+Fe3++ 等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫。
等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫。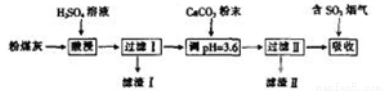
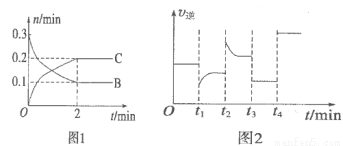
 xC(g) △H<0,B、C的物质的量随时间变化的关系如图l,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2。下列有关说法正确的是
xC(g) △H<0,B、C的物质的量随时间变化的关系如图l,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2。下列有关说法正确的是