题目内容
13.化学与环境保护有着密切关系,下列有关说法正确的是( )| A. | 积极开发和利用新能源,减少煤、石油等化石燃料的使用量 | |
| B. | 明矾净水的原理和家用消毒液消毒的原理相同 | |
| C. | 工业上燃烧煤时,加入少量石灰石是为了减少CO2的排放 | |
| D. | 雾霾的形成与工厂废气的排放有关,与汽车尾气无关 |
分析 A.新能源是清洁能源;
B.明矾净水的原理:明矾电离产生铝离子,铝离子水解生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性,所以能净水;“84”消毒液消毒的原理在水溶液中生成次氯酸,次氯酸的具有氧化作用可用于消毒;
C.加入少量的石灰石,二氧化硫可转化为硫酸钙;
D.汽车尾气中含有大量有害物体和粉尘.
解答 解:A.积极开发和利用新能源,减少化石能源的开采,减少了环境污染,能保护环境,故A正确;
B.明矾净水的原理:明矾电离产生铝离子,铝离子水解生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性,所以能净水;“84”消毒液消毒的原理在水溶液中生成次氯酸,次氯酸的具有氧化作用可用于消毒,两者的原理不同,故B错误;
C.加入少量的石灰石,二氧化硫可转化为硫酸钙,可减少二氧化硫的污染,故C错误;
D.汽车尾气中含有大量有害物体和粉尘,所以汽车尾气随意排放,与雾霾形成有很大的关系,故D错误.
故选A.
点评 本题考查较为综合,涉及环境污染、明矾净水等知识,为高考常见题型,侧重于基础知识的综合理解和运用的考查,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列除杂试剂、主要操作或方法均正确的是(括号内为杂质)( )
| 选项 | 原物质及杂质 | 除杂试剂 | 主要操作或方法 |
| A | 乙酸乙酯(乙酸) | Na2CO3 | 过滤 |
| B | Na2CO3(s )[NaHCO3(s )] | NaOH溶液 | 转化法 |
| C | FeCl2(CuCl2) | Zn | 过滤 |
| D | 苯(溴) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
1.工业制硝酸的主要反应是:4NH3(g)+5O2(g)?4NO(g)+6H2O (g)+1025kJ
(1)该反应的平衡常数表达式为$\frac{{c}^{4}(NO){c}^{6}({H}_{2}O)}{{c}^{4}(N{H}_{3}){c}^{5}({O}_{2})}$;升高温度K值减小 (填“增大”、“减小”或“不变”).
(2)若反应物起始的物质的量相同,下列关系图错误的是c (填字母序号).
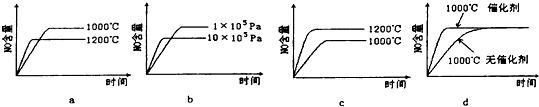
(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①起始时物料比c (O2):c (NH3)>1.25,其原因是增大氨气的转化率.
②反应在第2min到第4min时O2的平均反应速率为0.1875;
③反应在第8min改变的反应条件可能是增大反应物的浓度.
(1)该反应的平衡常数表达式为$\frac{{c}^{4}(NO){c}^{6}({H}_{2}O)}{{c}^{4}(N{H}_{3}){c}^{5}({O}_{2})}$;升高温度K值减小 (填“增大”、“减小”或“不变”).
(2)若反应物起始的物质的量相同,下列关系图错误的是c (填字母序号).

(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.8 | 0.975 | 0.5 |
②反应在第2min到第4min时O2的平均反应速率为0.1875;
③反应在第8min改变的反应条件可能是增大反应物的浓度.
8.下列叙述正确的是( )
| A. | 在原电池的负极和电解池的阴极上都发生失电子的氧化反应 | |
| B. | 用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 | |
| C. | 用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH | |
| D. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
5.下列物质分类正确的是( )
| A. | 碱:纯碱、烧碱 | B. | 纯净物:氨水、液态氧 | ||
| C. | 盐:KClO3、小苏打 | D. | 混合物:盐酸、液氯 |
2.下列反应中,硝酸既表现氧化性又表现酸性的是( )
| A. | FeO和HNO3 | B. | Cu(OH)2和HNO3 | C. | CuO和HNO3 | D. | H2S和HNO3 |
3.下列关于Na及其化合物的性质描述正确的是( )
| A. | Na的密度小于K的密度,故K与水反应,K不会浮在水面上 | |
| B. | Na2O2具有强氧化性,用途上可用做漂白剂 | |
| C. | Na2CO3俗称“小苏打”,可用于治疗胃酸过多 | |
| D. | K-Na合金因为具有很强的还原性,故可用作原子反应堆的导热剂 |
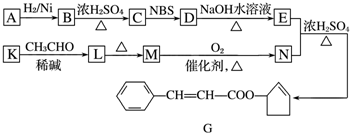
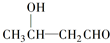
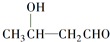 $\stackrel{△}{→}$CH3CH═CHCHO+H2O
$\stackrel{△}{→}$CH3CH═CHCHO+H2O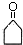 ,G中官能团的名称为碳碳双键和酯基.
,G中官能团的名称为碳碳双键和酯基. ,反应类型加成反应.
,反应类型加成反应.


