题目内容
8.实验室用加热二氧化锰和浓盐酸制氯气,离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O若生成标况下2.24L Cl2,则被氧化的HCl的物质的量为0.2 mol.分析 实验室是用二氧化锰和浓盐酸反应制氯气,反应生成氯气、二氯化锰、水,依据离子方程式书写方法,易溶于水的强电解质拆成离子;依据n=$\frac{V}{{V}_{m}}$计算物质的量,结合化学方程式计算得到被氧化氯化氢,由此分析解答.
解答 解:实验室是用二氧化锰和浓盐酸反应制氯气,反应生成氯气、二氯化锰、水,反应的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O;生成标况下Cl2 2.24L,物质的量=$\frac{2.24L}{22.4L/mol}$=0.1mol,MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,反应中每生成1mol氯气,被氧化氯化氢为2mol,则生成
0.1mol氯气被氧化HCl物质的量为0.2mol,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O; 0.2 mol.
点评 本题考查化学方程式计算、氧化还原反应计算等,难度不大,注意参加反应的盐酸与被氧化的盐酸的物质的量的关系.

练习册系列答案
相关题目
18.能使H2O+H2O≒H3O++OH-的电离平衡向电离方向移动,但所得溶液仍呈中性的是( )
| A. | 加入硫酸 | B. | 加入少量氯化铵晶体 | ||
| C. | 继续加水 | D. | 升温 |
19.常温下,在下列溶液中可能大量共存的离子组是( )
| A. | pH=0的溶液:Fe2+、Mg2+、NO3-、SO42- | |
| B. | 由水电离出的c(H+)=1×10-13mol/L的溶液:Al3+、K+、SO42-、Cl- | |
| C. | $\frac{c({OH}^{-})}{c({H}^{+})}$=1012的溶液中:NH4+、Al3+、NO3-、CO32- | |
| D. | pH=14的溶液:Na+、K+、Al3+、CO32- |
3.已知:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O; Cl2+2FeCl2═2FeCl3; 2KI+2FeCl3═2KCl+I2+2FeCl2. 则下列判断正确的是( )
| A. | 氧化性MnO4->Cl2>I2>Fe3+ | B. | 还原性:Fe2+>I->Cl- | ||
| C. | Fe3+能将I-氧化为I2 | D. | Fe2+只有还原性 |
13.部分弱酸的电离平衡常数如下表:下列选项错误的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 ( 25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A. | 2CN-+H2O+CO2→2HCN+CO32- | |
| B. | 2HCOOH+CO32-→2HCOO-+H2O+CO2↑ | |
| C. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 | |
| D. | 等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者 |
20.下列化学用语正确的是( )
| A. | 硫酸铁的化学式为FeSO4 | |
| B. | 氧离子结构示意图: | |
| C. | 碳酸氢钠的电离方程式 NaHCO3═Na++HCO3- | |
| D. | 质量数为37的氯核素符号:${\;}_{37}^{17}$Cl |
17.将物质的量均为0.1molK2SO4和Al2(SO4)3溶于水,向其中加入一定量的Ba(OH)2溶液,测得铝元素有一半留在溶液中,则生成BaSO4的物质的量可能为( )
| A. | 0.25mol | B. | 0.30mol | C. | 0.35mol | D. | 0.4mol |
18.反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的为( )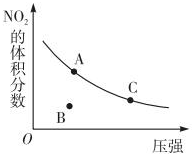

| A. | A、C两点的反应速率:v(A)>v(C) | |
| B. | A、C两点气体的颜色:A深,C浅 | |
| C. | B点正逆反应速率:v(正)>v(逆) | |
| D. | A、C两点气体的平均相对分子质量:A>C |
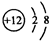 ,S2-的结构示意图
,S2-的结构示意图 .
.