题目内容
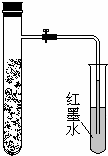 如图,向还原铁粉中加入少量的炭粉,混合均匀后,撒入内壁用NaCl溶液润湿过的具支试管中,塞紧橡皮塞.几分钟后,打开止水夹,观察到导管中水柱上升.对此过程所作的分析正确的是( )
如图,向还原铁粉中加入少量的炭粉,混合均匀后,撒入内壁用NaCl溶液润湿过的具支试管中,塞紧橡皮塞.几分钟后,打开止水夹,观察到导管中水柱上升.对此过程所作的分析正确的是( )| A、铁粉在电化学腐蚀过程中作正极 | B、炭粉被氧化 | C、发生了吸氧腐蚀 | D、发生了析氢腐蚀 |
分析:向还原铁粉中加入少量的炭粉,混合均匀后,撒入内壁用NaCl溶液润湿过的具支试管中,塞紧橡皮塞.几分钟后,打开止水夹,观察到导管中水柱上升,说明具支试管中气体压强减小,铁、碳和氯化钠溶液构成原电池,铁发生吸氧腐蚀.
解答:解:打开止水夹,观察到导管中水柱上升,说明具支试管中气体压强减小,铁、碳和氯化钠溶液构成原电池,
A.铁易失电子发生氧化反应而作负极,故A错误;
B.铁作负极、碳作正极,正极上氧气得电子发生还原反应,故B错误;
C.铁电极上铁失电子发生氧化反应,正极上氧气得电子生成氢氧根离子,所以该装置发生了吸氧腐蚀,故C正确;
D.如果发生析氢腐蚀,则具支试管中气体压强增大,会导致导管中液面下降,实际上液面上升,所以发生吸氧腐蚀,故D错误;
故选C.
A.铁易失电子发生氧化反应而作负极,故A错误;
B.铁作负极、碳作正极,正极上氧气得电子发生还原反应,故B错误;
C.铁电极上铁失电子发生氧化反应,正极上氧气得电子生成氢氧根离子,所以该装置发生了吸氧腐蚀,故C正确;
D.如果发生析氢腐蚀,则具支试管中气体压强增大,会导致导管中液面下降,实际上液面上升,所以发生吸氧腐蚀,故D错误;
故选C.
点评:本题考查了探究吸氧腐蚀,根据导管中液面变化确定具支试管中气体压强变化,从而确定发生吸氧腐蚀还是析氢腐蚀,注意吸氧腐蚀和析氢腐蚀的条件,题目难度不大.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
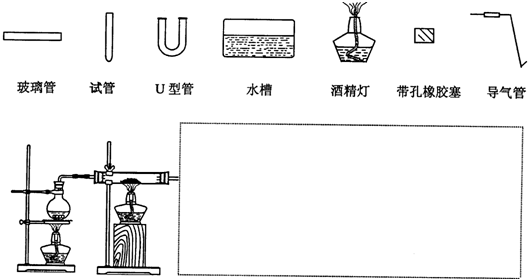
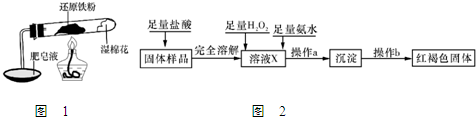
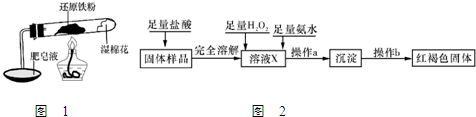
铁不能与冷、热水反应,但能与水蒸气反应.资料显示,在不同温度下,还原铁粉与水蒸气反应的产物是不同的,温度低于570℃时,生成FeO,高于570℃时,生成Fe3O4.老师用图1所示实验装置,完成还原铁粉与水蒸气反应的演示实验.
(1)实验中使用肥皂液的作用是 .
(2)甲同学为探究实验后试管内的固体含有哪些物质,进行了下列实验:
根据上述实验,能确定固体中存在的物质是 ;不能确定是否存在Fe3O4的原因是
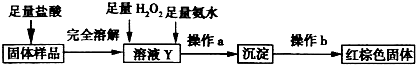
(3 )乙同学设计实验方案如图2以确定实验后试管内的固体是否存在Fe3O4:
①溶液X中发生氧化还原反应的离子方程式为 ;足量氨水与金属离子反应的离子方程式为 .
②操作a包括过滤和洗涤,检验沉淀是否已经洗涤干净的操作是 .
③确定是否存在Fe3O4需要测定并记录的实验数据是 .
(1)实验中使用肥皂液的作用是 .
(2)甲同学为探究实验后试管内的固体含有哪些物质,进行了下列实验:
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈绿色;有少量气泡产生 |
| ② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
(3 )乙同学设计实验方案如图2以确定实验后试管内的固体是否存在Fe3O4:
①溶液X中发生氧化还原反应的离子方程式为 ;足量氨水与金属离子反应的离子方程式为 .
②操作a包括过滤和洗涤,检验沉淀是否已经洗涤干净的操作是 .
③确定是否存在Fe3O4需要测定并记录的实验数据是 .

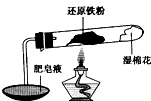 在高温条件下铁与水能发生反应.资料显示,在不同温度下,还原铁粉与水蒸气反应的产物是不同的,温度低于570℃时,生成Fe0,高于570℃时,生成Fe304.老师用如图所示实验装置,完成还原铁粉与水蒸气反应的演示实验.
在高温条件下铁与水能发生反应.资料显示,在不同温度下,还原铁粉与水蒸气反应的产物是不同的,温度低于570℃时,生成Fe0,高于570℃时,生成Fe304.老师用如图所示实验装置,完成还原铁粉与水蒸气反应的演示实验.