题目内容
12.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图 I~IV所示.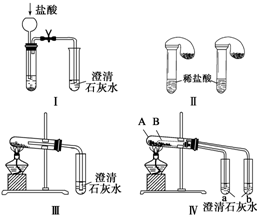
(1)只根据图 I、II所示实验,能够达到实验目的是(填装置序号)Ⅱ.
(2)图 III、IV所示实验均能鉴别这两种物质,其反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;与实验 III 相比,实验 IV的优点是(填选项序号)D.
A. III比 IV复杂 B. IV比 III安全
C. IV比 III操作简便 D. IV可以做到用一套装置同时进行两个对比实验,而 III不行
(3)若用实验V验证酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是(填化学式)NaHCO3.
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应.
①当石灰水过量时,其离子方程式为HCO3+OH-+Ca2+═CaCO3↓+H2O;②碳酸氢钠与氢氧化钙的物质的量之比是2:1时,所得溶液中的溶质的化学式为Na2CO3.
分析 (1)碳酸钠和盐酸反应分两步进行,盐酸和碳酸钠、碳酸氢钠反应都生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊.
(2)碳酸氢钠在加热条件下能分解生成碳酸钠和水、二氧化碳;根据两个实验的区别分析.
(3)根据碳酸氢钠的性质分析.
(4)碳酸氢钠和氢氧化钙发生复分解反应,石灰水过量时反应生成碳酸钙、NaOH、水;碳酸氢钠与氢氧化钙的物质的量之比是2:1时,生成碳酸钙、碳酸钠和水.
解答 解:(1)Ⅰ装置反应现象相同;Ⅱ装置,向碳酸钠溶液中滴加盐酸先没有气体生成,随着盐酸的不断滴加,后产生气泡,向碳酸氢钠溶液中滴加盐酸立即产生气泡,所以能够达到实验目的是Ⅱ,
故答案为:Ⅱ;
(2)碳酸氢钠在加热条件下能分解生成碳酸钠和水、二氧化碳2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;实验Ⅲ、Ⅳ相比,IV可以做到一套装置同时进行两个对比实验,而III不能,故选D,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;D;
(3)碳酸钠直接加热不产生气体,而碳酸氢钠不直接加热就产生气体,就更说明碳酸氢钠不稳定,所以试管B中装入的固体最好是NaHCO3,
故答案为:NaHCO3;
(4)①当石灰水过量时,其离子方程式为HCO3+OH-+Ca2+═CaCO3↓+H2O,故答案为:HCO3+OH-+Ca2+═CaCO3↓+H2O;
②碳酸氢钠与氢氧化钙的物质的量之比是2:1时,发生2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O,所得溶液中的溶质的化学式为,故答案为:Na2CO3.
点评 本题考查性质实验方案的设计,为高频考点,把握碳酸钠、碳酸氢钠的性质及差异、实验装置的作用为解答的关键,侧重分析与实验能力的考查,题目难度不大.

 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案| A. | 二氧化硫具有还原性,可用二氧化硫水溶液吸收溴蒸气 | |
| B. | 氢氟酸具有强酸性,可用氢氟酸蚀刻玻璃 | |
| C. | 氨气具有氧化性,可用浓氨水检验氯气管道是否泄漏 | |
| D. | SiO2的导电能力强,可用于制造通讯光缆 |
| A. | 当△H为“-”时,表示该反应为吸热反应 | |
| B. | 反应热的大小与反应物所具有的能量和生成物所具有的能量无关 | |
| C. | 化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关 | |
| D. | 由热化学方程式H2(g)+F2(g)═2HF(g)△H=-270 kJ/mol可知2 L氟化氢气体分解成1 L的氢气和1 L的氟气吸收270 kJ热量 |
| A. | O2 | B. | SO2 | C. | KCl | D. | KOH |
| A. | 工业上制取漂白粉:向澄清石灰水中通入足量的Cl2 | |
| B. | 验证醋酸是弱电解质:常温下测定0.1 mol•L-1醋酸钠溶液的pH | |
| C. | 探究FeCl3和KI溶液反应限度:向5mL0.1 mol•L-1 FeCl3溶液中加入0.1 mol•L-1KI溶液1mL,振荡,加苯萃取后,向水层中加入5滴KSCN溶液,观察实验现象 | |
| D. | 检验蔗糖水解生成的葡萄糖:蔗糖溶液在稀硫酸存在下水浴加热一段时间后,再与银氨溶液混合加热,观察实验现象 |