题目内容
14.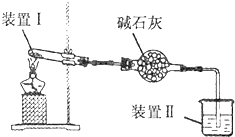 按如图所示装置进行实验,装置中现象II不正确的是( )
按如图所示装置进行实验,装置中现象II不正确的是( )| 选项 | 装置I中试剂 | 装置Ⅱ中试剂 | 装置Ⅱ中现象 |
| A | 浸透了石蜡油的石棉和碎瓷片 | 酸性高锰酸钾溶液 | 紫色溶液褪色 |
| B | 铁粉和用水浸泡的棉团 | 肥皂水 | 肥皂水冒泡 |
| C | 碳酸氢钠 | 澄清石灰水 | 有沉淀生成 |
| D | 硫酸铵 | 酚酞溶液 | 溶液变红 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.石蜡油在I中分解生成烯烃,烯烃能使酸性高锰酸钾溶液褪色;
B.加热条件下,Fe和水反应生成四氧化三铁和氢气,氢气不易溶于水;
C.碳酸氢钠分解生成碳酸钠、二氧化碳和水,二氧化碳、水能被碱石灰吸收;
D.加热条件下,硫酸铵分解生成氨气,氨气溶于水而使溶液呈碱性,碱遇酚酞试液变红色.
解答 解:A.石蜡油在I中分解生成烯烃,烯烃含有碳碳双键导致其性质较活泼,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故A正确;
B.加热条件下,Fe和水反应生成四氧化三铁和氢气,氢气不易溶于水,所以II中肥皂水冒泡,故B正确;
C.碳酸氢钠分解生成碳酸钠、二氧化碳和水,二氧化碳、水能被碱石灰吸收,所以II中不能产生白色沉淀,故C错误;
D.加热条件下,硫酸铵分解生成氨气,氨气溶于水而使溶液呈碱性,碱遇酚酞试液变红色,则II中溶液变红色,故D正确;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及物质反应、物质检验、气体干燥等知识点,明确实验原理及物质性质是解本题关键,题目难度不大.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
4.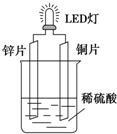 以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如图所示.某实验兴趣小组做完实验后,在读书卡片上记录如下:
以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如图所示.某实验兴趣小组做完实验后,在读书卡片上记录如下:
(1)在卡片上,记录合理的是⑤⑥(填序号).
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是锌片不纯(在锌片表面形成原电池).
(3)其他条件相同情况下,产生气泡的速率比单一锌片快(填“快”或“慢”),
如果将锌片换成铁片,电路中的电流方向不变(填“变”或“不变”).
(4)如果把硫酸换成硫酸铜溶液,猜测铜片(填“锌片”或“铜片”)变厚,原因是Cu2++2e-=Cu(用电极方程式表示).实验结束后称得两极质量差12.9g,假设初始时Zn片与Cu片质量相等,则反应中转移的电子的物质的量为0.2mol.
(5)有同学利用原电池原理,将A、B、C、D四种金属设计下表中装置进行实验用以判断四种金属的活泼性强弱.
根据以上现象,判断四种金属活泼性由强到弱的顺序是D>A>B>C.
 以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如图所示.某实验兴趣小组做完实验后,在读书卡片上记录如下:
以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如图所示.某实验兴趣小组做完实验后,在读书卡片上记录如下:| 实验后的记录: ①Zn片发生还原反应,Cu片发生氧化反应 ②H+向负极移动 ③LED发光时,电子流动方向Zn→导线→Cu,再经溶液流回铜片 ④溶液的pH变小 ⑤若有1mol电子流过导线,则产生H2为0.5mol. ⑥装置中存在“化学能→电能→光能”的转换 |
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是锌片不纯(在锌片表面形成原电池).
(3)其他条件相同情况下,产生气泡的速率比单一锌片快(填“快”或“慢”),
如果将锌片换成铁片,电路中的电流方向不变(填“变”或“不变”).
(4)如果把硫酸换成硫酸铜溶液,猜测铜片(填“锌片”或“铜片”)变厚,原因是Cu2++2e-=Cu(用电极方程式表示).实验结束后称得两极质量差12.9g,假设初始时Zn片与Cu片质量相等,则反应中转移的电子的物质的量为0.2mol.
(5)有同学利用原电池原理,将A、B、C、D四种金属设计下表中装置进行实验用以判断四种金属的活泼性强弱.
| 序号 | 甲 | 乙 | 丙 |
| 装置 | 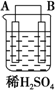 | 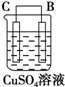 |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
5.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染.下列做法不符合绿色化学理念的是( )
| A. | 研制水溶剂涂料替代有机溶剂涂料 | |
| B. | 用可降解塑料生产包装盒或快餐盒 | |
| C. | 用反应:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O 制备硫酸铜 | |
| D. | 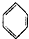 +CH2=CH2→ +CH2=CH2→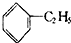 |
9.氨气溶于水得到氨水,氯气溶于水得到氯水,下列关于新制的氨水、氯水的描述不正确的是( )
| A. | “两水”都能与FeCl2溶液反应 | |
| B. | “两水”中都存在可逆反应 | |
| C. | “两水”都有刺激性气味 | |
| D. | “两水”都是混合物,溶液中含有的粒子种类数相同 |
19.金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高强度和铝的低密度.其单质和化合物具有广泛的应用价值.氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品.以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图1).
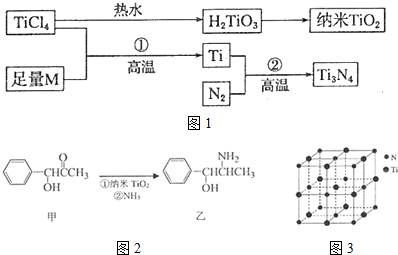
图中的M是短周期金属元素,M的部分电离能如下表:
请回答下列问题:
(1)Ti的基态原子外围电子排布式为3d24s2;
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X一射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.则KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为TiN>CaO>KCl.判断依据是:离子所带的电荷数越高,晶格能越大,熔点越高.

图中的M是短周期金属元素,M的部分电离能如下表:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/kJ•mol-1 | 738 | 1451 | 7733 | 10540 | 13630 |
(1)Ti的基态原子外围电子排布式为3d24s2;
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X一射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.则KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为TiN>CaO>KCl.判断依据是:离子所带的电荷数越高,晶格能越大,熔点越高.
3.现有Na2CO3、H2SO4、Ba(OH)2三种溶液,它们的体积与物质的量浓度都相等.以不同顺序将它们中的两种混合,若产生沉淀则过滤,再将滤液与第三种溶液混合,那么最终所得的溶液( )
| A. | 可能呈酸性 | B. | 不可能呈碱性 | ||
| C. | 可能呈中性或碱性 | D. | 不可能呈中性 |
4.下列说法或实验操作正确的是( )
| A. | 容量瓶、量筒和滴定管上都标有使用温度,容量瓶无“0”刻度,量筒、滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| B. | 向3支试管中各加入2mL 0.1mol•L-1酸性高锰酸钾溶液和2mL 0.01mol•L-1 H2C2O4溶液,将它们分别置于冰水、室温下、80℃热水中,观察比较褪色快慢 | |
| C. | 皂化反应结束后的混合液中加入饱和食盐水,再通过分液操作分离出硬脂酸钠 | |
| D. | 为保证实验安全,金属钠切割下来的表层物质应放回原试剂瓶,不能在研钵中研磨氯酸钾或硝酸钾 |
 .
. (填结构简式).
(填结构简式).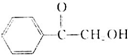 )的合成路线.
)的合成路线.