题目内容
19.对如图两种化合物的结构或性质描述错误的是( )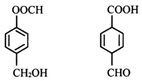
| A. | 均可发生取代、加成反应 | |
| B. | 均能使酸性高锰酸钾溶液褪色 | |
| C. | 分子中共平面的碳原子数相同 | |
| D. | 互为同分异构体,可用NaHCO3溶液鉴别 |
分析 前者含-COOCH、-OH,后者含碳碳双键、-COOH、-OH,结合酯、烯烃、羧酸、醇的性质来解答.
解答 解:A.含-OH、-COOH均可发生取代反应,含苯环、碳碳双键可发生加成反应,故A正确;
B.前者含-OH,后者含-CHO、双键,均能使酸性高锰酸钾溶液褪色,故B正确;
C.苯环为平面结构,前者有8个C原子共面,后者碳碳双键为平面结构,与-CHO、-COOH相连的C为四面体构型,则8个C不可能共面,故C错误;
D.分子式相同、结构不同,互为同分异构体,后者含-COOH,与NaHCO3溶液反应,用NaHCO3溶液鉴别,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意常见有机物性质的应用,题目难度不大.

练习册系列答案
相关题目
14.下列事实中,能说明HNO2是弱电解质的是( )
| A. | HNO2溶液用水稀释后,H+浓度下降 | |
| B. | HNO2溶液的导电性比盐酸弱 | |
| C. | HNO2溶液不与氯化钠反应 | |
| D. | 0.lmol•L-1的HNO2溶液的c(H+)=l0-2mol/L |
15.几种短周期元素的原子半径及主要化合价如表:
下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/nm | 0.160 | 0.143 | 0.070 | 0.066 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | 元素的金属性:X<Y | |
| B. | 原子Z的价电子数为5 | |
| C. | 元素的简单离子半径:r(X2+)>r(W2-) | |
| D. | 元素Y的最高价氧化物对应的水化物能溶于氨水 |
7.有A、B、C、D、E五种原子序数小于18的元素,其特征信息如下表:
请回答下列问题:
(1)A、B、C三种元素形成的化合物含有的化学键类型是离子键、(极性)共价键.
(2)由A、B、C元素中两两组合形成的化合物相互反应生成单质的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.
(3)D单质与A、E形成的化合物的水溶液反应的离子方程式是2Al+6H+=2Al3++3H2↑.
(4)写出实验室制取单质E的化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(5)C和D两元素形成的单质活泼性较强的是(写元素符号)Na,你的判断依据是Na可与冷水剧烈反应,Al不与水反应.
| 元素编号 | 特征信息 |
| A | 有一种原子内只有质子,没有中子 |
| B | L层电子数是K层的3倍 |
| C | 其阳离子与B的阴离子具有相同的电子层结构,且核电荷数与B相差3 |
| D | 最外层电子数等于电子层数,且是地壳中含量较多的元素之一 |
| E | 单质为黄绿色,可用于制造漂白粉 |
(1)A、B、C三种元素形成的化合物含有的化学键类型是离子键、(极性)共价键.
(2)由A、B、C元素中两两组合形成的化合物相互反应生成单质的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.
(3)D单质与A、E形成的化合物的水溶液反应的离子方程式是2Al+6H+=2Al3++3H2↑.
(4)写出实验室制取单质E的化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(5)C和D两元素形成的单质活泼性较强的是(写元素符号)Na,你的判断依据是Na可与冷水剧烈反应,Al不与水反应.
4.短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的最高正价与最低负价的代数和为2,Y是地壳中含量最多的元素,Z原子的最外层电子数是Y原子的最外层电子数的一半,W与Y同主族.下列说法正确的是( )
| A. | 原子半径:r(X)<r(Y)<r(Z)<r(W) | |
| B. | 元素X、Y组成的化合物只有两种 | |
| C. | W的简单气态氢化物的热稳定性比Y的弱 | |
| D. | Q、Z的简单离子具有相同的电子层结构 |
11.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 500mL0.l mol/LFeCl3溶液中含Fe3+0.05NA | |
| B. | 常温常压下,2.24L氯气溶于NaOH溶液中,转移电子数为0.lNA | |
| C. | 常温常压下,28g乙烯中所含C-H键的数目为4NA | |
| D. | 0.5 mol锌与浓硫酸完全反应生成SO2和H2的混合气体(不考虑气体溶解),气体的分子总数小于0.5NA |
8.利用如图所示的装置可将CO2转化为燃料甲醇,下列说法正确的是( )


| A. | b极发生还原反应 | |
| B. | a极的电极反应:CH3OH+H2O-6e-═CO2+6H+ | |
| C. | 总反应方程式为:2CO2+4H2O$\frac{\underline{\;通电\;}}{\;}$2CH3OH+3O2 | |
| D. | 该装置将化学能转变为电能 |
1.不同元素的原子在分子内吸引电子的能力大小可用一数值X来表示,若X越大,则原子吸引电子的能力越强,在所形成的分子中成为负电荷一方.下面是某些短周期元素的X值.
(1)通过分析X值的变化规律,确定N、Mg的X值范围:0.93<X(Mg)<1.57;2.55<X(N)<3.44.
(2)推测X值与原子半径的关系是同周期(或同主族)元素,x值越大,原子半径越小.
(3)某有机物结构简式为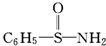 ,在S~N中,你认为共用电子对偏向谁?氮(写原子名称).
,在S~N中,你认为共用电子对偏向谁?氮(写原子名称).
(4)经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为离子键,当△X<1.7时,一般为共价键,试推断AlBr3中化学键的类型是共价键
(5)预测元素周期表中,X值最小的元素位置第六周期第ⅠA族(放射性元素除外).
| 元素 | Li | Be | B | C | O | F |
| X值 | 0.98 | 1.57 | 2.04 | 2.53 | 3.44 | 3.98 |
| 元素 | Na | Al | Si | P | S | Cl |
| X值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(2)推测X值与原子半径的关系是同周期(或同主族)元素,x值越大,原子半径越小.
(3)某有机物结构简式为
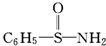 ,在S~N中,你认为共用电子对偏向谁?氮(写原子名称).
,在S~N中,你认为共用电子对偏向谁?氮(写原子名称).(4)经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为离子键,当△X<1.7时,一般为共价键,试推断AlBr3中化学键的类型是共价键
(5)预测元素周期表中,X值最小的元素位置第六周期第ⅠA族(放射性元素除外).