题目内容
下列说法中,正确的是
A.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
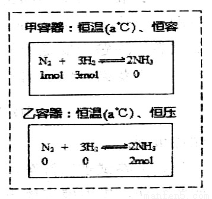
B.通过上图所示的不同途径,可建立相同的平衡,但反应过程中放出或吸收的热量可能不相等
C.C(石墨,s)=C(金刚石,s) △H> 0所以金刚石比石墨稳定
D.水的电离过程是吸热过程,升高温度,水的离子积增大、pH增大
B
【解析】
试题分析:A、化学方程式确定时,反应热只与物质的聚集状态有关,与反应条件无关,所以点燃与光照条件下H2(g)+Cl2(g)=2HCl(g)的反应热相同,错误;B、甲容器是从正反应开始的平衡,而乙容器是从逆反应开始的平衡,所以二者放出或吸收的热量可能不相等,正确;C、石墨转化为金刚石是吸热反应,石墨石墨的能量低于金刚石,所以石墨稳定,错误;D、水的电离过程是吸热过程,升高温度,水的离子积增大,氢离子浓度增大,pH减小,错误,答案选B。
考点:考查化学反应与能量的关系,物质稳定性的判断,电离平衡的移动与pH的变化

练习册系列答案
相关题目
 —
—

 ________(填“>”“=”或“<”)
________(填“>”“=”或“<”) 。
。