题目内容
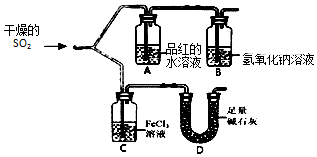
4.2016年8月的eLife上发表了浙江医科大学第二医院和浙江大学肿瘤研究所的晁明和胡汛等人的一篇论文.媒体以“用十几块钱的小苏打饿死了癌细胞”为题予以报道,报道曲解了小苏打的作用,但小苏打在他们治疗癌症的方法中确实功不可没.在实验室中模拟工业制取NaHCO3的实验步骤如下:①连接好装置,检验气密性,在仪器内装入药品.
②先让某一装置发生反应,直到产生的气体不能再在C中溶解,再通入另一装置中产生的气体,片刻后,C中出现固体.继续向C中通入两种气体,直到不再有固体产生.
③分离C中所得的混合物,得到NaHCO3固体.
④向滤液中加入适量的某固体粉末,有NH4Cl晶体析出.
(1)如图所示装置的连接顺序是:a接f;e接d;b接c(填接口编号).
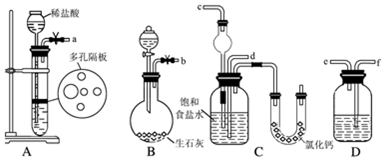
(2)A中反应的离子方程式为CaCO3+2H+=Ca2-+H2O+CO2↑;B中常选用的液体反应物为浓氨水;D中应选用的液体为饱和碳酸氢钠溶液.
(3)步骤②让B装置先发生反应.
(4)C中用球形干燥管而不用直导管,其作用是防倒吸;装有无水CaCl2的U形管的作用是吸收多余的NH3.
(5)步骤③分离出NaHCO3固体的操作是过滤.
(6)步骤④中所加固体粉末化学式为NaCl.所得的晶体中常含有少量的NaCl和NaHCO3(约占5%~8%),请设计一个简单的实验,不使用其他任何试剂,证明所得晶体大部分是NH4C1.简要写出操作和现象取少量固体放入试管中,加热,固体大部分消失,在试管口内壁又有较多的固体凝结.
分析 (1)由装置可知:A制取CO2,制备的CO2中混有HCl,用装置D除去二氧化碳中的HCl,装置B制取NH3,二氧化碳与氨气通入C中,其中氨气应防止倒吸,据此分析连接仪器装置;
(2)A装置是制备二氧化碳气体一般用碳酸钙和盐酸反应生成,二氧化碳气体中含有氯化氢气体,会影响碳酸氢钠的生成,D为装置除杂可以用饱和碳酸氢钠溶液,B装置用浓氨水制备氨气;
(3)氨气易溶于水,二氧化碳在水中的溶解度较小,制取碳酸氢钠时先要得到含氨的饱和食盐水;
(4)C中用球形干燥管球形部分空间大,液面上升缓慢,起缓冲作用,所以不用直导管;装有无水CaCl2的U形管的作用吸收多余的NH3;
(5)分离NaHCO3固体通常用过滤操作;
(6)为了析出氯化铵晶体,则向滤液中加入适量的NaCl粉末,提高氯离子浓度,使NH4Cl晶体析出;实验证明所得固体的成分大部分是氯化铵,是利用氯化铵的性质,受热生成氯化氢和氨气气体,在试管口处温度降低重新生成固体氯化铵分析判断.
解答 解:(1)A制取CO2,制备的CO2中混有HCl,用装置D除去二氧化碳中的HCl,为除杂充分,导气管应长进短出,故a连接f,装置B制取NH3,二氧化碳与氨气通入C中,氨气极易溶于水,故要注意防止倒吸,则e连接d,b连接c;
故答案为:f;e;d; c;
(2)A装置为固液制备二氧化碳,实验室常用碳酸钙和盐酸反应生成,离子方程式为:CaCO3+2H+=Ca2-+H2O+CO2↑,生成的二氧化碳气体中含有氯化氢,若不除去碳酸氢钠难以形成,所以应用饱和碳酸氢钠溶液或饱和氯化钠溶液除去;B装置为浓氨水滴入生石灰制备氨气;
故答案为:CaCO3+2H+=Ca2-+H2O+CO2↑;浓氨水;饱和碳酸氢钠溶液;
(3)候氏制碱方法是利用氨气溶解性大极易溶解于水,二氧化碳气体水中溶解性较小,实验饱和食盐水中先通入氨气,再通入二氧化碳气体;实验操作过程中,应让B装置先发生反应;
故答案为:B;
(4)氨气极易溶于水,用直导管向饱和氯化钠溶液中通入氨气,容易发生倒吸,C中用球形干燥管球形部分液面上升慢起缓冲作用,可以防止倒吸;装有无水CaCl2的U形管的作用吸收多余的NH3;
故答案为:防倒吸;吸收多余的NH3;
(5)分离NaHCO3固体和液体用过滤的方法;
故答案为:过滤;
(6)第四步中为了析出氯化铵晶体,则向滤液中加入适量的NaCl粉末,提高氯离子浓度,使NH4Cl晶体析出;所得固体的成分大部分是氯化铵,是利用氯化铵的分解产物为气体,温度降低氨气和氯化氢气体会重新生成固体氯化氨,方法为:取少量固体放入试管中,加热,固体大部分消失,在试管口内壁又有较多的固体凝结,从而证明所得固体的成分大部分是氯化铵;
故答案为:NaCl;取少量固体放入试管中,加热,固体大部分消失,在试管口内壁又有较多的固体凝结.
点评 本题考查了实验制备碳酸氢钠的过程分析和装置作用判断,掌握候氏制碱的反应原理和反应特征是解题关键,熟练掌握工业制备流程和注意问题,能顺利解决问题,侧重于考查学生的分析问题和解决问题的能力,注意相关基础知识的学习与积累.

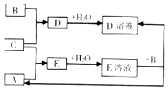 短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )
短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )| A. | 化合物YX中含离子键 | B. | Z的含氧酸均为强酸 | ||
| C. | 非金属性:X>Z | D. | 离子半径:Y>Z |
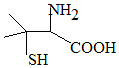 靑霉素是最重要的抗生素,其在体内经酸性水解后得到一种有机物X.己知X的结构如图,下列有关X的说法正确的是( )
靑霉素是最重要的抗生素,其在体内经酸性水解后得到一种有机物X.己知X的结构如图,下列有关X的说法正确的是( )| A. | X为烃的含氧衍生物 | |
| B. | X的分子式为C5H10NO2S | |
| C. | X只能发生取代反应 | |
| D. | X中碳原子上的H若有1个被Cl取代,有2种不同产物 |
| A. | 金属钠和氧气反应,条件不同,产物则不同 | |
| B. | 钠长期放置在空气中,最终将变成碳酸钠 | |
| C. | 钠的化学性质比较活泼,少量的钠可以保存在与钠不反应的煤油中 | |
| D. | 将一小块钠投入氯化铁溶液时,既能产生气体又会出现白色沉淀 |
| A. | KClO3→KCI | B. | HNO3→NO | C. | Mn2+→Mn04- | D. | Fe3+→Fe2+ |
| A. | 沸点:F2<Cl2<Br2 | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 碱性:KOH>NaOH>Mg(OH)2 | D. | 离子半径:Na+>F->O2- |