题目内容
下列拟采用的金属防腐措施,不正确的是( )
| A、给金属衣架或电线外面包上一层塑料层 |
| B、给自行车钢圈镀上一层金属铬 |
| C、在铁船身上镶嵌金属铜 |
| D、给铁栅栏表面涂上一层油漆 |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:金属的防护措施有牺牲阳极的阴极保护法、外加电流的阴极保护法,另外还有电镀、喷镀、喷油漆等方法使金属与空气、水等物质隔离,以防止金属腐蚀.
解答:
解:A、衣架和电线的外面包上一层塑料层属于外加防护膜的保护法,可以隔绝空气而防止生锈,故A正确;
B、给自行车钢圈镀上一层金属铬,是改变金属的内部结构,可以防止生锈,故B正确;
C、在铁船身上镶嵌金属铜,由于金属铁比铜活泼,形成原电池时,Fe作负极失电子,被腐蚀,故C错误;
D、给铁栅栏表面涂上一层油漆属于外加防护膜的保护法,可以隔绝空气而防止生锈,故D正确;
故选C.
B、给自行车钢圈镀上一层金属铬,是改变金属的内部结构,可以防止生锈,故B正确;
C、在铁船身上镶嵌金属铜,由于金属铁比铜活泼,形成原电池时,Fe作负极失电子,被腐蚀,故C错误;
D、给铁栅栏表面涂上一层油漆属于外加防护膜的保护法,可以隔绝空气而防止生锈,故D正确;
故选C.
点评:本题考查了金属的腐蚀与防护,明确金属生锈原理是解本题关键,把握减慢金属生锈的方法,难度不大.

练习册系列答案
相关题目
以下各常数随着温度的升高不一定增大的是( )
| A、Kw | B、K | C、Ka | D、Kb |
24mL 0.05mol/L的Na2SO3溶液,恰好与20mL 0.02mol/L的K2Cr2O7溶液完全反应,已知Na2SO3被氧化为Na2SO4,则元素Cr在被还原的产物中的化合价是( )
| A、+2 | B、+3 | C、+4 | D、+5 |
有关如图所示装置的叙述不正确的是( )
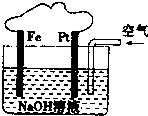

| A、该装置内可发生原电池反应 |
| B、该装置中Pt为正极,电极反应为:O2+2H2O+4e-=4OH- |
| C、溶液中会出现红褐色的沉淀 |
| D、该装置中Fe为阴极,电极反应为:Fe-2e-+2OH-=Fe(OH)2 |
已知燃烧1mol葡萄糖(Mr=180)的放出的热量是2804kJ?mol-1,当氧化1g葡萄糖时放出的热量是( )
| A、51.9kJ |
| B、15.6kJ |
| C、155.8kJ |
| D、26.0kJ |
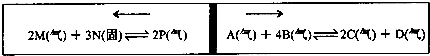
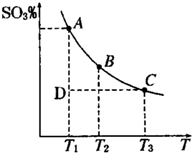 运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义.