题目内容
设NA为阿伏加德岁常数,下列叙述正确的是( )
| A、1L 0.1 mol?L-1碳酸钠溶液中的阴离子总数为0.1NA |
| B、将400 mL 1 mol/L的HNO3溶液与7 g Fe粉充分反应,转移电子数为0.375NA |
| C、标准状况下,14 g氮气中共用电子对的数目为1.5NA |
| D、已知反应N2(g)+3H2(g)?2NH3(g)△H=-91.8KJ/mol中反应物的转化率为30%,相同条件下,当放出91.8 kJ热量时,生成氨分子的数目为0.6NA |
考点:阿伏加德罗常数
专题:
分析:A.碳酸根离子部分水解,导致溶液中阴离子总数增大;
B.7g铁的物质的量为0.125mol,根据n=cV计算出硝酸的物质的量,然后根据反应Fe+4H++NO3-=Fe3++NO↑+2H2O判断铁粉完全转化成铁离子时消耗硝酸的物质的量,从而得出硝酸不足,转移的电子小于0.375mol;
C.氮气分子中含有3对共用电子对,14g氮气的物质的量为0.5mol,含有1.5mol共用电子对;
D.根据热化学方程式可知,放出91.8 kJ热量时会生成2mol氨气.
B.7g铁的物质的量为0.125mol,根据n=cV计算出硝酸的物质的量,然后根据反应Fe+4H++NO3-=Fe3++NO↑+2H2O判断铁粉完全转化成铁离子时消耗硝酸的物质的量,从而得出硝酸不足,转移的电子小于0.375mol;
C.氮气分子中含有3对共用电子对,14g氮气的物质的量为0.5mol,含有1.5mol共用电子对;
D.根据热化学方程式可知,放出91.8 kJ热量时会生成2mol氨气.
解答:
解:A.1L 0.1 mol?L-1碳酸钠溶液中含有溶质碳酸钠0.1mol,由于碳酸根离子部分水解,导致溶液中阴离子数目增大,则溶液中含有的阴离子的物质的量大于0.1mol,含有的阴离子总数大于0.1NA,故A错误;
B.400 mL 1 mol/L的HNO3溶液中含有0.4mol硝酸,7gFe粉的物质的量为:
=0.125mol,0.125mol铁粉完全反应生成铁离子时转移0.375mol电子,根据离子方程式Fe+4H++NO3-=Fe3++NO↑+2H2O可知,0.125mol铁粉完全反应生成铁离子需要消耗硝酸的物质的量为:0.125mol×4=0.5mol,显然硝酸不足,转移的电子小于0.375mol,故B错误;
C.14g氮气的物质的量为0.5mol,0.5mol氮气中含有1.5mol共用电子对,共用电子对的数目为1.5NA,故C正确;
D.反应N2(g)+3H2(g)?2NH3(g)△H=-91.8KJ/mol中,放出91.8 kJ热量时会生成2mol氨气,生成氨分子的数目为2NA,故D错误;
故选C.
B.400 mL 1 mol/L的HNO3溶液中含有0.4mol硝酸,7gFe粉的物质的量为:
| 7g |
| 56g/mol |
C.14g氮气的物质的量为0.5mol,0.5mol氮气中含有1.5mol共用电子对,共用电子对的数目为1.5NA,故C正确;
D.反应N2(g)+3H2(g)?2NH3(g)△H=-91.8KJ/mol中,放出91.8 kJ热量时会生成2mol氨气,生成氨分子的数目为2NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确可逆反应特点,选项B为易错点,需要判断过量情况,根据不足量计算出转移电子数目.

练习册系列答案
相关题目
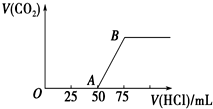 向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图所示.
向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图所示.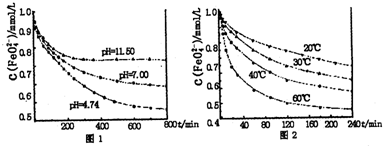
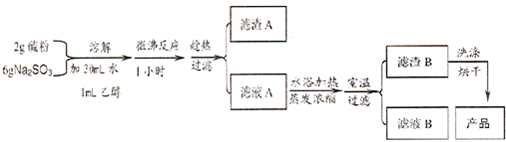

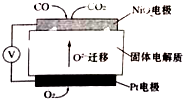 汽车尾气中的主要污染物是NO以及燃料不完全燃烧所产生的CO,它们是现代化城市中的大气污染物.为了减轻大气污染,人们提出通过以下反应来处理汽车尾气:2NO(g)+2CO(g)
汽车尾气中的主要污染物是NO以及燃料不完全燃烧所产生的CO,它们是现代化城市中的大气污染物.为了减轻大气污染,人们提出通过以下反应来处理汽车尾气:2NO(g)+2CO(g)
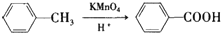
 (苯胺,易被氧化)
(苯胺,易被氧化)