题目内容
 有X、Y、Z、T、U五种短周期元素.X、Y、Z三元素在周期表中的位置如图所示,三元素的原子序数之和是41.X和T的单质在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄色固体)两种化合物.U单质在Z单质中燃烧时产生苍白色火焰,生成物的水溶液能使石蕊试液变红.
有X、Y、Z、T、U五种短周期元素.X、Y、Z三元素在周期表中的位置如图所示,三元素的原子序数之和是41.X和T的单质在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄色固体)两种化合物.U单质在Z单质中燃烧时产生苍白色火焰,生成物的水溶液能使石蕊试液变红.(1)各元素的符号是X
(2)Y原子的结构示意图为
(3)元素Y和Z中,非金属性较强的是
(4)用电子式表示Y与T组成的化合物的形成过程
(5)YX2和U2Y反应的化学方程式
(6)均由X、Y、T、U四种元素组成的两种盐反应生成一种易形成酸雨的气体,则该反应的离子反应方程式
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、T、U为5种短周期元素,X、Y、Z三种元素原子序数之和是41,由三元素在周期表中位置可知,不能是第一、二周期元素,分别为二、三周期元素,令x的原子序数为a,则Y、Z的原子序数分别为a+8、a+9,则a+a+8+a+9=41,解得a=8,则X为氧、Y为硫、Z为Cl,X和T的单质在不同条件下反应,可以生成化合物T2X(白色固体)和T2X2(淡黄色固体)两种化合物,则T为Na;U单质在Z单质中燃烧产生苍白色火焰,产物溶于水能使石蕊试液变红,则U为氢,据此解答.
解答:
解:X、Y、Z、T、U为5种短周期元素,X、Y、Z三种元素原子序数之和是41,由三元素在周期表中位置可知,不能是第一、二周期元素,分别为二、三周期元素,令x的原子序数为a,则Y、Z的原子序数分别为a+8、a+9,则a+a+8+a+9=41,解得a=8,则X为氧、Y为硫、Z为Cl,X和T的单质在不同条件下反应,可以生成化合物T2X(白色固体)和T2X2(淡黄色固体)两种化合物,则T为Na;U单质在Z单质中燃烧产生苍白色火焰,产物溶于水能使石蕊试液变红,则U为氢,
(1)由上述分析可知,X、U的元素符号分别为O、H,故答案为:O;H;
(2)Y为S元素,原子质子数为16,原子的结构示意图为 ,故答案为:
,故答案为: ;
;
(3)同周期自左而右元素非金属性增强,故元素Y和Z中,非金属性较强的是氯;其最高价氧化物对应水化物酸性较强的是HClO4,其对应离子的还原性较强的是S2-,其电子式为: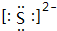 ,利用单质之间的相互置换可以验证,反应化学方程式为:Cl2+H2S=2HCl+S↓,
,利用单质之间的相互置换可以验证,反应化学方程式为:Cl2+H2S=2HCl+S↓,
故答案为:氯;HClO4;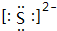 ;Cl2+H2S=2HCl+S↓;
;Cl2+H2S=2HCl+S↓;
(4)Y与T组成的化合物为Na2S,属于离子化合物,钠失去1个电子形成钠离子,S获得2个电子形成硫离子,用电子式表示Na2S的形成过程为: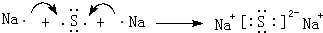 ,
,
故答案为: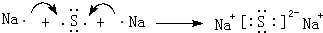 ;
;
(5)SO2和H2S反应的化学方程式为:2H2S+SO2═3S↓+2H2O,故答案为:2H2S+SO2═3S↓+2H2O;
(6)均由O、S、Na、h四种元素组成的两种盐反应生成一种易形成酸雨的气体,应是亚硫酸氢钠与硫酸氢钠反应生成硫酸钠、二氧化硫与水,则该反应的离子反应方程式为:H++HSO3-=H2O+SO2↑,
故答案为:H++HSO3-=H2O+SO2↑.
(1)由上述分析可知,X、U的元素符号分别为O、H,故答案为:O;H;
(2)Y为S元素,原子质子数为16,原子的结构示意图为
 ,故答案为:
,故答案为: ;
;(3)同周期自左而右元素非金属性增强,故元素Y和Z中,非金属性较强的是氯;其最高价氧化物对应水化物酸性较强的是HClO4,其对应离子的还原性较强的是S2-,其电子式为:
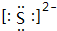 ,利用单质之间的相互置换可以验证,反应化学方程式为:Cl2+H2S=2HCl+S↓,
,利用单质之间的相互置换可以验证,反应化学方程式为:Cl2+H2S=2HCl+S↓,故答案为:氯;HClO4;
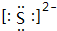 ;Cl2+H2S=2HCl+S↓;
;Cl2+H2S=2HCl+S↓;(4)Y与T组成的化合物为Na2S,属于离子化合物,钠失去1个电子形成钠离子,S获得2个电子形成硫离子,用电子式表示Na2S的形成过程为:
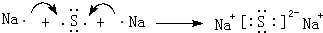 ,
,故答案为:
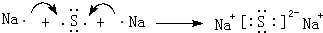 ;
;(5)SO2和H2S反应的化学方程式为:2H2S+SO2═3S↓+2H2O,故答案为:2H2S+SO2═3S↓+2H2O;
(6)均由O、S、Na、h四种元素组成的两种盐反应生成一种易形成酸雨的气体,应是亚硫酸氢钠与硫酸氢钠反应生成硫酸钠、二氧化硫与水,则该反应的离子反应方程式为:H++HSO3-=H2O+SO2↑,
故答案为:H++HSO3-=H2O+SO2↑.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,注意理解同主族元素原子序数关系,侧重对化学用语及元素化合物性质的考查,难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
下列物质所对应的化学式不正确的是( )
| A、纯碱-NaOH |
| B、重晶石-BaSO4 |
| C、过氧化钠-Na2O2 |
| D、硫化亚铁-FeS |
下列叙述正确的是( )
| A、工业上用电解熔融氯化钠的方法制取钠 |
| B、钠加入氯化镁的饱和溶液中可以制取金属镁 |
| C、电解冶炼铝的原料是氯化铝 |
| D、电解氯化镁溶液来制取镁 |
两种金属混合物粉末15g,与足量的盐酸反应时生成标准状况下11.2L氢气,符合上述情况的金属混合物是( )
| A、Zn、Fe |
| B、Zn、Ag |
| C、Al、Cu |
| D、Mg、Al |
元素周期表短周期的一部分,且M、X、Y、Z为主族元素,下列说法正确的是( )
| M | ||
| X | Y | Z |
| A、Y的氢化物的沸点一定比M的氢化物的沸点高 |
| B、Z的最高价氧化物对应的水化物有可能是弱电解质 |
| C、这四种元素形成的晶体单质都是分子晶体 |
| D、单质M的晶体中可能含有共价键和分子间作用力 |
实验室用MnO2和浓盐酸制氯气时,有14.6g HCl被氧化,所得氯气全部用石灰乳吸收,可制得漂白精的质量是( )
| A、14.3g |
| B、25.4g |
| C、28.6g |
| D、50.8g |
电解100mL 16%的氢氧化钠溶液(密度为1g/cm3),用石墨作电极,10min后电解液的浓度为19.5%,这是因为( )
| A、溶质增加了3.5g |
| B、氢氧化钠的物质的量不变,而水被电解了1mol |
| C、氢氧化钠的消耗比水的消耗少 |
| D、氢氧化钠不参加反应,只有水参加反应,且放出H2和O2,消耗了18g水 |
5.12克铜和一定质量的硝酸反应,当铜消耗完时,共收集到标准状况下的气体3.36升,若把装有这些气体的集气瓶倒立在盛水的水槽中,需通入多少升标准状况下的氧气才能使集气瓶充满溶液.( )
| A、0.336升 |
| B、0.224升 |
| C、0.896升 |
| D、1.12升 |
 4.53g硫酸铝铵晶体加热分解,最终剩余0.51g Al2O3固体.加热过程中,固体质量随温度的变化如图所示.请通过计算确定400℃时剩余固体成分的化学式(写出计算过程).
4.53g硫酸铝铵晶体加热分解,最终剩余0.51g Al2O3固体.加热过程中,固体质量随温度的变化如图所示.请通过计算确定400℃时剩余固体成分的化学式(写出计算过程).