题目内容
1.根据下图所给信息,得出的结论正确的是( )
| A. | 碳的燃烧热为b kJ/mol | B. | 2C(s)+O2(g)═2CO(g)△H=-2(b-a) kJ/mol | ||
| C. | 2CO2(s)═2CO(g)+O2(g)△H=+a kJ/mol | D. | C(s)+O2(g)═CO2(g)△H<-b kJ/mol |
分析 据图示可知,1molC燃烧生成CO放热b-aKJ,完全燃烧生成二氧化碳放热bKJ,1molCO燃烧生成1mol二氧化碳放热aKJ,据此分析.
解答 解:A、1molC完全燃烧生成二氧化碳固体放热bKJ,碳的燃烧热应该是1mol碳单质完全燃烧生成二氧化碳气体放出的热量,不是b kJ/mol,故A错误;
B、据图示可知,1molC燃烧生成CO放热b-aKJ,所以2molC燃烧生成CO放热2(b-a),故B正确;
C、1molCO燃烧生成1mol二氧化碳放热aKJ,所以2CO2(g)═2CO(g)+O2(g)△H=+2ak/mol,故C错误;
D、生成二氧化碳固体,△H=-b kJ/mol,但是固体转化为气体吸热,所以△H>-b kJ/mol,故D错误;
故选B.
点评 本题考查了据图象分析反应热的大小,注意热化学方程式中的物质状态,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.在下列4种化合物:①NaHCO3 ②Al2O3 ③(NH4)2S ④CH3COONH4中,跟盐酸和氢氧化钠溶液都能反应的是( )
| A. | 只有②④ | B. | 只有①② | C. | 只有①②③ | D. | ①②③④ |
2.某高分子化合物的部分结构如下: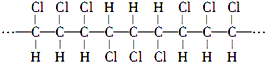 ;下列说法正确的是(双选)( )
;下列说法正确的是(双选)( )
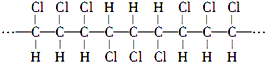 ;下列说法正确的是(双选)( )
;下列说法正确的是(双选)( )| A. | 聚合物的分子式是C3H3Cl3 | |
| B. | 聚合物的链节是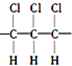 | |
| C. | 合成该聚合物的单体是CHCl═CHCl | |
| D. | 若n表示聚合度,则其相对分子质量为97n |
9.化学使人类生活得更美好的一门自然科学.下列说法正确的是( )
| A. | 豆浆富含蛋白质,煮沸后蛋白质变成了氨基酸 | |
| B. | 浓硫酸可刻蚀石英制艺术品 | |
| C. | 氢氧化铝可作胃酸的中和剂 | |
| D. | 装饰材料中释放的甲醛、苯不会造成污染 |
16.下表是元素周期表的一部分,表中的每个字母代表一种短周期元素.
(1)a元素和b元素可以形成最简单的有机物,其化学式为CH4;
(2)e元素位于第三周期第ⅠA族,它的元素符号是Na;
(3)c元素原子的最外层电子数为5;
(4)b、c、d三种元素的非金属性逐渐增强(填“减弱”或“增强”);
(5)f的元素符号为S.
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | |||||||
| 2 | b | c | d | |||||
| 3 | e | f | ||||||
(2)e元素位于第三周期第ⅠA族,它的元素符号是Na;
(3)c元素原子的最外层电子数为5;
(4)b、c、d三种元素的非金属性逐渐增强(填“减弱”或“增强”);
(5)f的元素符号为S.
6.下列关于有机化合物的叙述中不正确的是( )
| A. | 丙烷跟甲烷一样能与氯气发生取代反应 | |
| B. | 相同条件,等物质的量的乙醇、乙二醇、丙三醇中分别加入足量的金属钠产生氢气的体积之比是2:3:6 | |
| C. | CH2Cl2只有一种结构说明甲烷是四面体结构而不是正方形结构 | |
| D. | 溴水既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷 |
13.如图装置可用来监测空气中NO的含量,下列说法不正确的是( )


| A. | 电子由Pt电极流出,经外电路流向NiO电极 | |
| B. | Pt电极上发生的是还原反应 | |
| C. | NiO电极的电极反应式为NO+O2--2e-═NO2 | |
| D. | 每转移2 mol电子,有1 mol O2-迁移到负极 |
10.下列叙述不正确的是( )
| A. | 生理盐水的浓度为0.9% | |
| B. | 阿司匹林具有解热镇痛的作用 | |
| C. | 垃圾是放错地方的资源,应分类回收利用 | |
| D. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
11.银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-═ZnO+H2O;Ag2O+H2O+2e-═2Ag+2OH-;总反应为:Ag2O+Zn═2Ag+ZnO,下列判断正确的是( )
| A. | 锌为正极,Ag2O为负极 | |
| B. | 如果有1mol电子转移,就有32.5g Zn参加反应 | |
| C. | 原电池工作时,正极区PH减小 | |
| D. | 锌为阳极,Ag2O为阴极 |