题目内容
18.太阳能电池板材料除单晶硅外,还有铜、硒、氮、硼、镓、镁、钙等化学物质.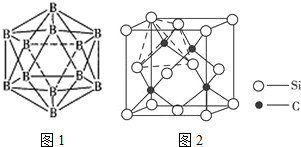
(1)亚铜离子(Cu+)基态时的价电子排布式为3d10;
(2)氮元素的第一电离能在同周期中从大到小排第3位;写出与NO${\;}_{3}^{-}$互为等电子体的一种非极性分子化学式SO3等;
(3)H2Se的酸性比H2S强(填“强”或“弱”).
(4)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图1),其中有两个原子为10B,其余为11B,则该结构单元有3种不同的结构类型.
(5)如图2为碳化硅的晶胞(其中●为碳原子,○为硅原子).
①三个碳原子和三个硅原子相间构成一个椅式(船、椅)六元环.
②如果我们以一个硅原子为中心,则与硅原子次近的第二层有12个原子.
③已知:碳原子半径为a×10-8cm,硅子半径为b×10-8cm,假设碳、硅原子是刚性小球,在晶体中彼此相切,计算碳化硅晶体的密度为$\frac{160}{{N}_{A}×[\frac{4(a+b)}{\sqrt{3}}×1{0}^{-8}]^{3}}$g/cm3(只要求列出算式),查表知该密度比实测值偏小,其原因可能是密度偏小,说明实际晶胞的体积下小于计算值,实际上碳、硅原子之间形成共价键,而不是相切,碳、硅原子间的距离比两个原子半径之和小.
(6)在浓的CrCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为CrCl3•6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配离子的化学式为[TiCl(H2O)5]2+.
(7)难溶碳酸盐受热易分解,试比较MgCO3和CaCO3的稳定性,并说明理由稳定性:CaCO3>MgCO3,碳酸盐的热分解是由于晶体中的阳离子结合碳酸根离子中的氧离子,使碳酸根离子分解为二氧化碳分子的结果,产物中氧化镁和氧化钙都为离子晶体,因为镁离子半径小于钙离子半径则氧化镁晶格能大,更稳定,更易于生成.
分析 (1)Cu原子价电子排布式为3d104s1,失去4s能级的1个电子形成Cu+;
(2)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于同周期相邻元素的,稀有气体的第一电离能最大;
原子数目相等、价电子总数也相等的微粒互为等电子体,分子中正负电荷重心重合的分子属于非极性分子(中心原子价电子全部成键);
(3)Se的原子半径大于S的,故H-Se不如H-S键稳定;
(4)两个10B有3位置,为图中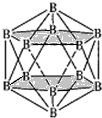 上下顶点位置,其中一个处于上顶点,另外的一个处于上层阴影中顶点,或者下层阴影中顶点;
上下顶点位置,其中一个处于上顶点,另外的一个处于上层阴影中顶点,或者下层阴影中顶点;
(5)①三个碳原子和三个硅原子相间构成一个六元环为图中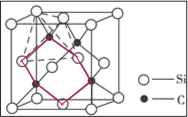 红线连接的原子,为椅式结构;
红线连接的原子,为椅式结构;
②距离中心Si最近的第一层的4个C原子,每一个又连接着另外3个Si原子;
③黑色球连接周围的4个白色球形成正四面体结构,黑色球位于正四面体的中心,黑色球与晶胞顶点白色球连线处于晶胞体对角线上,且二者之间距离为体对角线长度的$\frac{1}{4}$,而晶胞体对角线长度为晶胞棱长的$\sqrt{3}$倍,据此算晶胞棱长,根据均摊法计算晶胞中Si、C原子数目,表示出晶胞的质量,再根据ρ=$\frac{m}{V}$计算晶体密度;
Si、C原子之间形成共价键,原子间距小于二者原子半径之和,计算的体积比实际体积偏大;
(6)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3•6H20的绿色晶体,该晶体中两配体的物质的量之比为1:5,则配体中有1个Cl-、5个H2O,2个氯离子位于外界;
(7)分解生成金属氧化物,金属氧化物的晶格能大,更稳定,更易于生成.
解答 解:(1)Cu原子价电子排布式为3d104s1,失去4s能级的1个电子形成Cu+,Cu+基态时的价电子排布式为3d10,
故答案为:3d10;
(2)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于同周期相邻元素的,稀有气体的第一电离能最大,故第二周期第一电离能:Ne>F>N>O>C>Be>B>Li,
原子数目相等、价电子总数也相等的微粒互为等电子体,与NO3-互为等电子体的一种非极性分子化为SO3等,
故答案为:3;SO3等;
(3)Se的原子半径大于S的,故H-Se不如H-S键稳定,在溶液中更溶液电离,故H2Se的酸性比H2S强,
故答案为:强;
(4)两个10B有3位置,为图中 上下顶点位置,其中一个处于上顶点,另外的一个处于上层阴影中顶点,或者下层阴影中顶点,有3种结构,
上下顶点位置,其中一个处于上顶点,另外的一个处于上层阴影中顶点,或者下层阴影中顶点,有3种结构,
故答案为:3;
(5)①三个碳原子和三个硅原子相间构成一个六元环为图中 红线连接的原子,为椅式结构,
红线连接的原子,为椅式结构,
故答案为:椅;
②距离中心Si最近的第一层的4个C原子,每一个又连接着另外3个Si原子,则与硅原子次近的第二层有12个原子,
故答案为:12;
③黑色球连接周围的4个白色球形成正四面体结构,黑色球位于正四面体的中心,黑色球与晶胞顶点白色球连线处于晶胞体对角线上,且二者之间距离为体对角线长度的$\frac{1}{4}$,而晶胞体对角线长度为晶胞棱长的$\sqrt{3}$倍,故晶胞棱长为(a×10-8cm+b×10-8cm)×4÷$\sqrt{3}$,晶胞中C原子数目为4,Si原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,故晶胞质量为4×$\frac{12+28}{{N}_{A}}$g,故晶体密度为4×$\frac{12+28}{{N}_{A}}$g÷[(a×10-8cm+b×10-8cm)×4÷$\sqrt{3}$]3=$\frac{160}{{N}_{A}×[\frac{4(a+b)}{\sqrt{3}}×1{0}^{-8}]^{3}}$g/cm3,
密度偏小,说明实际晶胞的体积下小于计算值,实际上碳、硅原子之间形成共价键,而不是相切,碳、硅原子间的距离比两个原子半径之和小,
故答案为:$\frac{160}{{N}_{A}×[\frac{4(a+b)}{\sqrt{3}}×1{0}^{-8}]^{3}}$;密度偏小,说明实际晶胞的体积下小于计算值,实际上碳、硅原子之间形成共价键,而不是相切,碳、硅原子间的距离比两个原子半径之和小;
(6)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3•6H20的绿色晶体,该晶体中两配体的物质的量之比为1:5,则配体中有1个Cl-、5个H2O,2个氯离子位于外界,则该配离子的化学式为[TiCl(H2O)5]2+,
故答案为:[TiCl(H2O)5]2+;
(7)碳酸盐的热分解是由于晶体中的阳离子结合碳酸根离子中的氧离子,使碳酸根离子分解为二氧化碳分子的结果,产物中氧化镁和氧化钙都为离子晶体,因为镁离子半径小于钙离子半径则氧化镁晶格能大,更稳定,更易于生成,稳定性:CaCO3>MgCO3,
故答案为:稳定性:CaCO3>MgCO3,碳酸盐的热分解是由于晶体中的阳离子结合碳酸根离子中的氧离子,使碳酸根离子分解为二氧化碳分子的结果,产物中氧化镁和氧化钙都为离子晶体,因为镁离子半径小于钙离子半径则氧化镁晶格能大,更稳定,更易于生成.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、电离能、等电子体、晶胞计算与计算、配合物、晶格能等,是对学生综合能力的考查,难度较大.

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案| Y | Z | ||
| X | W |
| A. | 原子半径:X<Y<Z | |
| B. | 气态氢化物的稳定性:X>Z | |
| C. | 最高价氧化物对应水化物的酸性:Y>W | |
| D. | Z、W均可与Mg形成离子化合物 |
| A. | 根据原子核外电子排布的特点,Zn在周期表中属于ds区元素 | |
| B. | P4和CH4都是正四面体形分子且键角都为109°28′ | |
| C. | NH3分子中N原子和H2O分子中O原子的杂化类型不相同 | |
| D. | 原子间只通过共价键而形成的三维网状结构的晶体一定具有高的熔、沸点及硬度 |
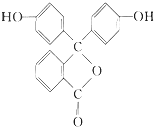
| A. | 酚酞具有弱酸性,且属于芳香烃 | |
| B. | 酚酞的分子式为C19H12O4 | |
| C. | 1mol酚酞最多与2molNaOH发生反应 | |
| D. | 酚酞在碱性条件下能够发生水解反应,呈现红色 |
| A. | 向 0.1 mol/L的氨水中加少量硫酸铵固体,则溶液中$\frac{c(O{H}^{-})}{(N{H}_{3}•{H}_{2}O)}$增大 | |
| B. | 常温下,0.1 mol/L一元酸(HA)溶液的 pH=3,则该溶液中,c2(H+)=c(H+)×c(A-)+Kw | |
| C. | 向含有 1 mol KAl(SO4)2 的溶液中加入 Ba(OH)2 溶液得到沉淀的物质的量最多为 2 mol | |
| D. | 将 Ca(ClO)2、Na2SO3、FeCl3、NaAlO2 溶液蒸干均得不到原溶质 |
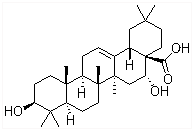 刺囊酸具有滋肝补血、凉血止血功能,结构式如图所示.下列关于刺囊酸的说法不正确的是( )
刺囊酸具有滋肝补血、凉血止血功能,结构式如图所示.下列关于刺囊酸的说法不正确的是( )| A. | 和氧所催化氧化后产物中含有醛基 | B. | 能和NaHCO3溶液反应生成CO2 | ||
| C. | 能使酸性高锰酸钾溶液褪色 | D. | 能发生取代、氧化、加成等反应 |
| A. | 碳原子数≤10 的烷烃,其一氯代物没有同分异构体的烷烃共有3种 | |
| B. | 烯烃、炔烃、芳香烃都能与溴水反应而使其褪色 | |
| C. | 等质量的CH≡CH和C6H6完全燃烧时消耗等物质的量的氧气 | |
| D. | 分子式为C6H12与C3H6的两种烃一定互为同系物 |
(1)第二周期中,元素的第一电离能处于B与N之间的元素有3种.
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为3d84s2.
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到.乙烯酮分子中碳原子杂化轨道类型是sp2和sp,1mol(C2H5O)3P=O分子中含有的σ键的数目为25NA.
(4)已知固态NH3、H2O、HF的氢键键能和结构如下:
| 物质 | 氢键X-H…Y | 键能kJ•mol-1 |
| (HF)n | D-H…F | 28.1 |
| 冰 | O-H…O | 18.8 |
| (NH3)n | N-H…N | 5.4 |
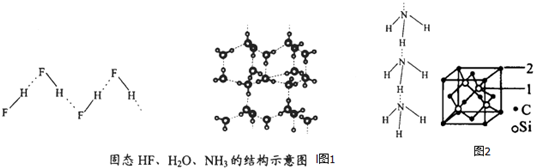
解释H2O、HF、NH3沸点依次降低的原因单个氢键的键能是(HF)n>冰>(NH3)n,而平均每个分子含氢键数:冰中2个,(HF)n和(NH3)n只有1个,气化要克服的氢键的总键能是冰>(HF)n>(NH3)n.
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能.碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有4个,与碳原子等距离最近的碳原子有12个.已知碳化硅晶胞边长为apm,则晶胞图中1号硅原子和2号碳原子之间的距离为$\frac{\sqrt{11}a}{4}$pm,碳化硅的密度为$\frac{1.6×1{0}^{32}}{{a}^{3}×{N}_{A}}$g/cm3.
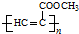 .
.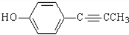 .
.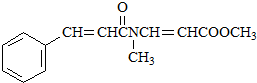 .
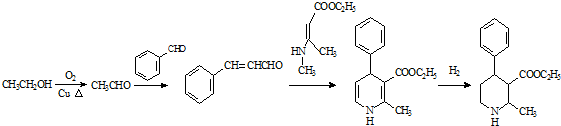
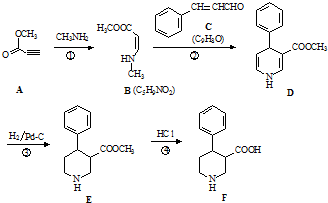
.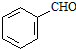 、CH3CH2OH和
、CH3CH2OH和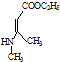 为原料,合成
为原料,合成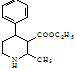 ,写出合成流程图(无机试剂任用).
,写出合成流程图(无机试剂任用).