题目内容
3.现用该浓硫酸配制100mL1.000mol/L的稀硫酸.可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒;⑧100mL容量瓶.请回答:①配制稀硫酸时,上述仪器中需要使用的除①③⑤外,还有⑦⑧(填序号).
②下列操作会使配制的溶液浓度偏高的是B.
A.量取浓H2SO4时,俯视刻度线
B.定容时,俯视容量瓶刻度线
C.配置前,容量瓶中有水珠
D.定容后摇匀发现液面下降,但未向其中再加水.
分析 ①根据配制一定物质的量浓度溶液的实验步骤确定操作所需仪器;
②分析操作对溶质的物质的量和溶液体积的影响,根据c=$\frac{n}{V}$进行误差分析,凡是使溶质的物质的量偏大或者溶液体积偏小的操作,溶液浓度都偏高,据此解答.
解答 解:①配制100mL 1.000mol/L的稀硫酸,可用量筒量取一定体积的浓硫酸,在烧杯中加水稀释,冷却后转移到100mL容量瓶中,并用玻璃棒引流,并洗涤烧杯,将洗涤液一并转移到容量瓶中,加入蒸馏水至刻度线2~3cm时,改用教头滴管定容,则还需要的仪器有玻璃棒和100mL容量瓶,
故答案为:⑦⑧;
②A.量取浓H2SO4时,俯视刻度线,会导致量取液体体积偏小,浓度偏低,故A错误;
B.定容时,俯视容量瓶刻度线,会导致体积偏小,浓度偏大,故B正确;
C.配制前,容量瓶中有水珠,对实验没有影响,故C错误;
D.定容后摇匀发现液面下降而未向其中再加水,浓度没有影响,故D错误;
故答案为:B.
点评 本题考查了一定物质的量浓度溶液的配制及误差分析,明确配制原理及操作对溶质的物质的量和溶液体积的影响是解题关键,题目难度不大.

练习册系列答案
相关题目
11.下列有关元素周期表说法正确的是( )
| A. | 第 IA族元素都是碱金属元素 | |
| B. | 元素原子的最外层电子数等于它的族序数 | |
| C. | 最外层电子数相同的元素不一定在同一个族 | |
| D. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
18.在恒温、恒压的条件下,向可变容积的密闭容器中充入3LA和2LB,发生如下反应:3A(气)+2B(气)?xC(气)+yD(气)达到平衡时,C的体积分数为m%.若维持温度、压强不变,将0.6LA、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则x、y的值分别为( )
| A. | x=3 y=l | B. | x=4 y=1 | C. | x=5 y=1 | D. | x=2 y=3 |
12.将10molA和5molB放入10L真空容器内,某温度下发生反应:3A(g)+B(g)?2C(g),在最初的2min内,消耗A 3.6mol,则在2min时,C的平均速率是( )
| A. | 0.12mol/(L•min) | B. | 0.18 mol/(L•min) | C. | 1.8 mol/(L•min) | D. | 1.2mol/(L•min) |
13.下列有关化学用语的表述正确的是( )
| A. | CO2的比例模型: | |
| B. | N2H4的电子式为: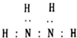 | |
| C. | NaH中氢离子结构示意图为: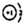 | |
| D. | 质子数是82,中子数是122的铅原子:${\;}_{82}^{122}$Pb |
 利用如图所示的装置和其他必要的仪器用品,完成下列实验.
利用如图所示的装置和其他必要的仪器用品,完成下列实验.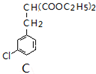 $\underset{\stackrel{①O{H}^{-},②{H}_{3}{O}^{+}}{→}}{③△}$D$\stackrel{SOCl_{2}}{→}$
$\underset{\stackrel{①O{H}^{-},②{H}_{3}{O}^{+}}{→}}{③△}$D$\stackrel{SOCl_{2}}{→}$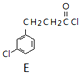 $\stackrel{AlCl_{3}}{→}$
$\stackrel{AlCl_{3}}{→}$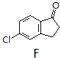
 或
或 (任写一种).
(任写一种). .
. 氯化苄是一种无色或微黄色的透明液体,是一种重要的化工、医药中间体.它的结构如图所示,则氯化苄完全氢化后所得到的有机物质在核磁共振氢谱图中有多少个吸收峰( )
氯化苄是一种无色或微黄色的透明液体,是一种重要的化工、医药中间体.它的结构如图所示,则氯化苄完全氢化后所得到的有机物质在核磁共振氢谱图中有多少个吸收峰( )