题目内容
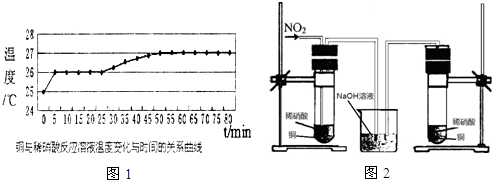
1.下列实验能达到实验目的是( )| A. | 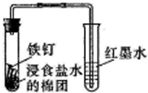 观察铁的吸氧腐蚀 | B. | 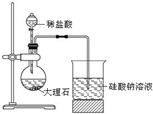 比较氯、碳、硅的非金属性 | ||
| C. | 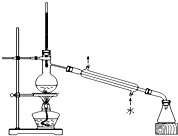 实验室蒸馏石油 | D. | 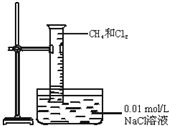 甲烷与氯气的取代反应 |
分析 A.食盐水为中性,发生吸氧腐蚀,右侧红墨水沿着导管上升;
B.盐酸易挥发,盐酸与硅酸钠溶液反应;
C.蒸馏中温度计测定馏分温度、冷却水下进上出;
D.0.01mol/L食盐水不是饱和溶液,氯气可溶解,且该实验需要光照.
解答 解:A.如果Fe发生吸氧腐蚀,会导致左边试管中压强减小,右边试管导气管中液面会上升,所以图中装置可观察铁的吸氧腐蚀,故A正确;
B.盐酸易挥发,盐酸与硅酸钠溶液反应,则图中装置不能比较碳、硅的非金属性,故B错误;
C.蒸馏中温度计测定馏分温度、冷却水下进上出,则图中蒸馏实验装置合理,故C正确;
D.0.01mol/L食盐水不是饱和溶液,氯气可溶解,且该实验需要光照,则试管中液面上升也不能验证取代反应的发生,故D错误;
故选AC.
点评 本题考查化学实验方案的评价,为高频考点,涉及电化学腐蚀、混合物分离提纯实验、常见有机物性质等,把握物质的性质及实验装置图的作用、反应原理为解答的关键,注意实验方案的评价性、操作性分析,题目难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
11.X、Y、Z均为短周期元素,其中两种为金属元素,一种为非金属元素,其原子半径分别为
X、Y处于同一周期,三种元素形成的简单离子具有相同的电子层结构.下列说法正确的是( )
| X | Y | Z | |
| 原子半径/nm | 0.154 | 0.130 | 0.071 |
| A. | 原子最外层电子数:Z>X>Y | B. | 三种元素可能为同周期元素 | ||
| C. | 原子序数:Y>X>Z | D. | 离子半径:X>Y>Z |
12.下列说法正确的是( )
| A. | (NH4)2SO4和CuSO4溶液都能使蛋白质沉淀析出 | |
| B. | 苯酚与甲醛在酸性条件下生成酚醛树脂的结构简式为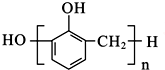 | |
| C. | 醋酸和硬脂酸互为同系物,C6H12和C9H18也一定互为同系物 | |
| D. | 迷迭香酸的结构为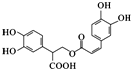 它可以发生酯化、水解但不能加成反应. 它可以发生酯化、水解但不能加成反应. |
9.下列物质属于电解质且能导电的是( )
| A. | 石墨 | B. | 液态HCl | C. | 葡萄糖 | D. | 熔融的Na2CO3 |
13.RbH是一种离子化合物,它跟水反应的方程式为:RbH+H2O=RbOH+H2↑,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气,下列有关RbH的叙述错误的是( )
| A. | 灼烧RbH时,火焰有特殊颜色 | |
| B. | RbH中H+半径比Li+半径小 | |
| C. | 跟液氨反应时,有RbNH2生成 | |
| D. | 在Na、K、Rb三种单质中,Rb的熔点最高 |
10.经验规律:当成键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当差值小于1.7时,一般为共价键.下列判断正确的是( )
| A. | AlCl3为离子化合物 | B. | Mg与Cl形成共价键 | ||
| C. | SiCl4为共价化合物 | D. | K与Mg 形成共价键 |