题目内容
8.饮茶是中国人的传统饮食文化之一.为方便饮用,可通过以下方法制取罐装饮料茶: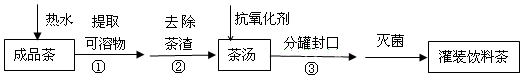
关于上述过程涉及的实验方法、实验操作和物质作用中说法不正确的是( )
| A. | ①是萃取 | B. | ②是过滤 | ||
| C. | ③是分液 | D. | 维生素C可作抗氧化剂 |
分析 由流程可知,热水溶解后,①为萃取,②为分离不溶性茶渣,②为过滤,对滤液加抗氧化剂后密封、灭菌,以此来解答.
解答 解:A.①提取可溶物,加有机溶解萃取,故A正确;
B.②为分离不溶性茶渣,②为过滤,故B正确;
C.③中混合物不分层,分罐密封,无分液操作,故C错误;
D.维生素C具有还原性,可作抗氧化剂,故D正确;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、流程中混合物分离方法、实验技能等为解答的关键,侧重分析与实验能力的考查,注意分液分离分层的液体混合物,题目难度不大.

练习册系列答案
相关题目
16.下列说法正确的是( )
| A. | 同周期的ⅡA族与ⅢA族元素的原子序数一定相差1 | |
| B. | 镁、铝、铜、铁、钠五种金属元素中,铜和铁属于过渡元素 | |
| C. | 元素的非金属性越强,其气态氢化物水溶液的酸性越强 | |
| D. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 |
13.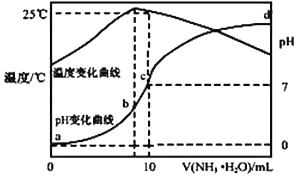 在某温度时,将 n mol•L-1氨水滴入 10mL 1.0mol•L-1 盐酸中,溶液 pH 和温度随加入氨 水体积变化曲线如图所示,下列有关说法正确的是( )
在某温度时,将 n mol•L-1氨水滴入 10mL 1.0mol•L-1 盐酸中,溶液 pH 和温度随加入氨 水体积变化曲线如图所示,下列有关说法正确的是( )
 在某温度时,将 n mol•L-1氨水滴入 10mL 1.0mol•L-1 盐酸中,溶液 pH 和温度随加入氨 水体积变化曲线如图所示,下列有关说法正确的是( )
在某温度时,将 n mol•L-1氨水滴入 10mL 1.0mol•L-1 盐酸中,溶液 pH 和温度随加入氨 水体积变化曲线如图所示,下列有关说法正确的是( )| A. | a 点 Kw=1.0×10-14 | |
| B. | 水的电离程度:b>c>a>d | |
| C. | b 点:c(NH4+)>c(Cl-)>c(H +)>c(OH -) | |
| D. | 25℃时 NH4Cl 水解常数为(10n-1)×10-7mol•L-1(用 n 表示) |
20.下列说法正确的是( )
| A. | 纳米铁粉可以高效地去除被污染水体中的 Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子有较强的物理吸附 | |
| B. | 凡含有添加剂的食物对人体健康均有害,不宜食用 | |
| C. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| D. | 火力发电中,燃烧是使化学能转换为电能的关键 |
7. 合成氨工业是我省开磷集团的重要支柱产业之一.氨是一种重要的化工原料,在工农业生产中有广泛的应用.
合成氨工业是我省开磷集团的重要支柱产业之一.氨是一种重要的化工原料,在工农业生产中有广泛的应用.
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2?2NH3.该可逆反应达到平衡的标志是C;
A.3v(H2)正=2v(NH3)逆
B.单位时间生成mmolN2的同时生成3mmolH2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间变化
(2)氨气具有还原性,例如,氨气能与卤素单质发生置换反应.已知几种化学键的键能数据如表所示:
请写出氨气与溴蒸汽反应的热化学方程式2NH3 (g)+3Br2(g)=N2(g)+6HBr(g)△H=-214KJ/mol;
(3)工业上可用天然气为原料来制取合成氨的原料气氢气.某研究性学习小组的同学模拟工业制取氨气的原理,在一定温度下,体积为2L的恒容密闭容器中,测得如下表所示数据.请回答下列问题:
①分析标准数据,判断5min时反应是否处于平衡状态(填“是”或“否”),前5min反应的平均反应速率v(CH4)=0.02mol•min-1;
②该温度下,上述反应的平衡常数K=0.0675;
③反应在7-10min内,CO的物质的量减少的原因可能是D(填字母)
A.减少CH4的物质的量 B.降低温度 C.升高温度 D.充入H2
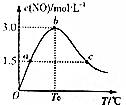
(4)氨的催化氧化:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)是工业制硝酸的重要反应.在1L密闭容器中充入4molNH3(g)和5molO2(g),保持其他条件不变,测得c(NO)与温度的关系如图所示.该反应的△H<0(填“>”、“<”
或“=”);T0温度下,NH3的转化率为75%.
 合成氨工业是我省开磷集团的重要支柱产业之一.氨是一种重要的化工原料,在工农业生产中有广泛的应用.
合成氨工业是我省开磷集团的重要支柱产业之一.氨是一种重要的化工原料,在工农业生产中有广泛的应用.(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2?2NH3.该可逆反应达到平衡的标志是C;
A.3v(H2)正=2v(NH3)逆
B.单位时间生成mmolN2的同时生成3mmolH2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间变化
(2)氨气具有还原性,例如,氨气能与卤素单质发生置换反应.已知几种化学键的键能数据如表所示:
请写出氨气与溴蒸汽反应的热化学方程式2NH3 (g)+3Br2(g)=N2(g)+6HBr(g)△H=-214KJ/mol;
| 化学键 | N-H | N≡N | Br-Br | H-Br |
| 键能/kJ•mol-1 | 391 | 946 | 194 | 366 |
| 时间/min | CH4(mol) | H2O(mol) | CO (mol) | H2 (mol) |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | a | 0.80 | c | 0.60 |
| 7 | 0.20 | b | 0.20 | d |
| 10 | 0.21 | 0.81 | 0.19 | 0.64 |
②该温度下,上述反应的平衡常数K=0.0675;
③反应在7-10min内,CO的物质的量减少的原因可能是D(填字母)
A.减少CH4的物质的量 B.降低温度 C.升高温度 D.充入H2
(4)氨的催化氧化:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)是工业制硝酸的重要反应.在1L密闭容器中充入4molNH3(g)和5molO2(g),保持其他条件不变,测得c(NO)与温度的关系如图所示.该反应的△H<0(填“>”、“<”
或“=”);T0温度下,NH3的转化率为75%.
 ;
; ;
;
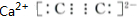 .
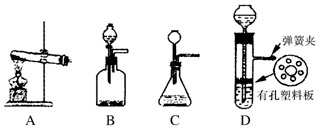
.
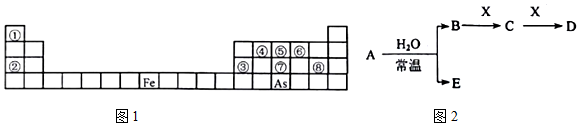
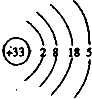 ;其氢化物的化学式为AsH3.
;其氢化物的化学式为AsH3.