题目内容
6.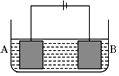 按如图所示的装置进行电解实验.A极是铜镍合金,B极为纯铜,电解质溶液为硫酸铜溶液(足量).通电一段时间后,A极恰好全部溶解,此时B极质量增加3.2g,溶液质量增加0.05g,(已知氧化性,Cu2+>Ni2+)则A合金中铜、镍原子个数比为( )
按如图所示的装置进行电解实验.A极是铜镍合金,B极为纯铜,电解质溶液为硫酸铜溶液(足量).通电一段时间后,A极恰好全部溶解,此时B极质量增加3.2g,溶液质量增加0.05g,(已知氧化性,Cu2+>Ni2+)则A合金中铜、镍原子个数比为( )| A. | 4:1 | B. | 3:1 | C. | 2:1 | D. | 1:1 |
分析 B极质量增加3.2g,电极反应式为:Cu2++2e-=Cu,也就是生成铜3.2g,物质的量为0.05mol,所以A极失去电子的物质的量为:0.05×2=0.1mol,开始电解总的反应式为:Ni+Cu2+$\frac{\underline{\;通电\;}}{\;}$Ni2++Cu,溶液质量增加64-59=5,所以当溶液质量增加0.05g时参加反应的0.01mol,而A极镍与铜共转移电子为0.1mol,所以铜转移电子为:0.1-0.01×2=0.08mol,则铜的物质的量为0.04mol,由此分析解答.
解答 解:B极质量增加3.2g,电极反应式为:Cu2++2e-=Cu,也就是生成铜3.2g,物质的量为0.05mol,所以A极失去电子的物质的量为:0.05×2=0.1mol,开始电解总的反应式为:Ni+Cu2+$\frac{\underline{\;通电\;}}{\;}$Ni2++Cu,溶液质量增加64-59=5,所以当溶液质量增加0.05g时参加反应的0.01mol,而A极镍与铜共转移电子为0.1mol,所以铜转移电子为:0.1-0.01×2=0.08mol,则铜的物质的量为0.04mol,则A合金中铜、镍原子个数比为0.04:0.01=4:1,
故选A.
点评 本题考查电解原理,侧重于电解的计算,注意把握两极的变化,从守恒的角度解答该题,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.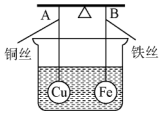 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )| A. | 杠杆为导体和绝缘体时,均为A端高B端低 | |
| B. | 杠杆为导体和绝缘体时,均为A端低B端高 | |
| C. | 当标杆为绝缘体时,A端低B端高;为导体时,A端高B端低 | |
| D. | 当标杆为绝缘体时,A端高B端低;为导体时,A端低B端高 |
8.YBa2Cu8Ox(Y为元素钇)是一种重要超导材料,下列关于${\;}_{39}^{89}$Y的说法错误的是( )
| A. | 质量数是89 | B. | 质子数与中子数之差为50 | ||
| C. | 核外电子数是39 | D. | ${\;}_{39}^{89}$Y与${\;}_{39}^{90}$Y互为同位素 |
14.25℃时,对下列各溶液的叙述中正确的是( )
| A. | pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| B. | 4种pH相同的溶液:①CH3COONa ②C6H5ONa ③NaHCO3 ④NaOH,各溶液的物质的量浓度由大到小的顺序是③>②>①>④ | |
| C. | 0.1 mol•L-1HA(某酸)的pH=3,0.1 mol•L-1 BOH(某碱)的pH=13,则BA(盐)溶液的pH<7 | |
| D. | pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2:1 |
1.称取(NH4)2SO4和NH4HSO4混合物样品7.24g,加入含0.1mol NaOH的溶液,完全反应后加热,生成NH3 1792mL(标准状况),则下列说法正确的是( )
| A. | NaOH只与NH4HSO4反应 | |
| B. | (NH4)2SO4在水中的电离方程式:(NH4)2SO4=NH4++SO42- | |
| C. | NH4HSO4的物质的量是0.04 mol | |
| D. | (NH4)2SO4和NH4HSO4物质的量之比是1.87:1 |
11.某温度下,在一个2L的密闭容器中加入4mol A和 2mol B进行如下反应:3A(g)+2B(g)?4C(s)+D(g),反应2min 后达到平衡,测得生成1.6mol C,下列说法正确的是( )
| A. | 前2 min,D的平均反应速率为0.2 mol•L-1•min-1 | |
| B. | 此时,B的平衡转化率是40% | |
| C. | 增大该体系的压强,平衡不移动,化学平衡常数不变 | |
| D. | 增加B,平衡向右移动,B的平衡转化率增大 |
18.某溶液中加入Al粉有H2放出,在该溶液中可能大量共存的离子组是( )
| A. | Na+、SO42-、Cl-、NO3- | B. | K+、Fe3+、Cl-、SCN- | ||
| C. | H+、Mg2+、SO42-、NO3- | D. | Al3+、K+、HS-、Na+ |
15. H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )
 H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )| A. | 过程 1 放热 | B. | 过程 2 吸热 | C. | 过程 3 放热 | D. | 过程 4 放热 |
16.下列实验操作、现象和解释或结论均正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将铝片分別加入浓HNO3和NaOH浓溶液中 | NaOH浓溶液中的铝片溶解 | 铝不与浓HNO3反应 |
| B | 向紫色石蕊试液中通入足量二氧化硫 | 溶液由紫色变为红色 | 二氧化硫与水反应有酸性物质生成 |
| C | 将分别蘸有浓氨水和浓硝酸的两根玻璃棒相互靠近 | 有白烟生成 | 浓硝酸具有强氧化性 |
| D | 向待测液中加入盐酸酸化的硝酸钡溶液 | 有白色沉淀生成 | 待测液中含有SO42- |
| A. | A | B. | B | C. | C | D. | D |