题目内容
6.下列电离方程式中,正确的是( )| A. | FeCl3=Fe2++3Cl- | B. | NaOH=Na++OH- | ||
| C. | H2SO4=H2++SO42- | D. | NaHCO3=Na++H++CO32- |
分析 选项中物质均为强电解质,均完全电离,弱酸的酸式酸根离子不能拆分,结合离子符号及电荷守恒来解答.
解答 解:A.FeCl3为强电解质,电离方程式为FeCl3=Fe3++3Cl-,故A错误
B.NaOH为强电解质,电离方程式为NaOH=Na++OH-,故B正确;
C.H2SO4为强电解质,电离方程式为H2SO4=2H++SO42-,故C错误;
D.NaHCO3为强电解质,电离方程式为NaHCO3=Na++HCO3-,故D错误;
故选B.
点评 本题考查电离方程式的书写,为高频考点,把握电解质的强弱、离子符号、电荷守恒为解答的关键,侧重分析与应用能力的考查,注意酸根离子的写法,题目难度不大.

练习册系列答案
相关题目
17. 如图所示的Mg~H2O2电池以海水为电解质溶液,可用于驱动无人驾驶的潜航器.该电池工作时,下列说法正确的是( )
如图所示的Mg~H2O2电池以海水为电解质溶液,可用于驱动无人驾驶的潜航器.该电池工作时,下列说法正确的是( )
 如图所示的Mg~H2O2电池以海水为电解质溶液,可用于驱动无人驾驶的潜航器.该电池工作时,下列说法正确的是( )
如图所示的Mg~H2O2电池以海水为电解质溶液,可用于驱动无人驾驶的潜航器.该电池工作时,下列说法正确的是( )| A. | Mg电极是该电池的正极 | B. | H2O2在石墨电极上发生氧化反应 | ||
| C. | 石墨电极附近溶液的碱性增强 | D. | 溶液中Cl-向正极移动 |
14.下列过程或现象与盐类水解无关的是( )
| A. | 使用热的纯碱溶液去油污 | B. | 浓氨水有刺激性气味 | ||
| C. | 明矾、氯化铁常用于净水 | D. | 硫化钠溶液有臭味 |
11.下列离子方程式中,书写正确的是( )
| A. | 将少量铜屑溶解在浓硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| B. | 用氢氧化钠溶液吸收氯气:Cl2+2OH-═ClO-+H2O | |
| C. | 用足量氨水吸收二氧化硫:2OH-+SO2═SO42-+H2O | |
| D. | 将稀硫酸滴在铁片上:2Fe+6H+═2Fe3++3H2↑ |
15.下列反应的两种物质因为反应物用量不同或反应条件不同而生成不同的产物是( )
①Na和O2②S和O2③Al和NaOH④CO2和Ca(OH)2 ⑤Cu和HNO3⑥Fe和C12⑦Na2CO3和HCl.
①Na和O2②S和O2③Al和NaOH④CO2和Ca(OH)2 ⑤Cu和HNO3⑥Fe和C12⑦Na2CO3和HCl.
| A. | 全部 | B. | 除②、③、⑥外 | C. | 除②、④、⑦外 | D. | 除③、⑥、⑦外 |
15.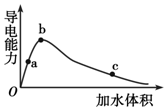 一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
 一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )| A. | 醋酸的电离程度:a<b<c | |
| B. | 溶液的pH值:b>a>c | |
| C. | 蘸取c点溶液滴在湿润的pH试纸上,测得pH值一定偏大 | |
| D. | 若分别向a、b、c三点的溶液中,加入同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a=b=c |