题目内容
从下列实验事实所得出的相应结论正确的是( )
| 实验事实 | 结论 | |
| ① | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| ② | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| ③ | NaHCO3溶液与Na[Al(OH)4]溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| ④ | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
| ⑤ | 某无色晶体加入氢氧化钠浓溶液中并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该晶体中一定有NH4+ |
| A、②③⑤ | B、①②③ |
| C、③④⑤ | D、①③⑤ |
考点:化学实验方案的评价
专题:
分析:①品红溶液褪色,气体为二氧化硫、氯气等;
②燃烧的镁条放入CO2中能继续燃烧,生成MgO和C;
③Na[Al(OH)4]溶液促进碳酸氢根离子的电离生成氢氧化铝沉淀和碳酸根离子;
④N≡N键能大,性质稳定;
⑤产生的气体能使湿润红色石蕊试纸变蓝,气体为氨气.
②燃烧的镁条放入CO2中能继续燃烧,生成MgO和C;
③Na[Al(OH)4]溶液促进碳酸氢根离子的电离生成氢氧化铝沉淀和碳酸根离子;
④N≡N键能大,性质稳定;
⑤产生的气体能使湿润红色石蕊试纸变蓝,气体为氨气.
解答:
解:①品红溶液褪色,气体为二氧化硫、氯气等,若加热恢复红色,气体为二氧化硫,故错误;
②燃烧的镁条放入CO2中能继续燃烧,生成MgO和C,由还原剂的还原性大于还原产物的还原性可知,还原性为Mg>C,故正确;
③Na[Al(OH)4]溶液促进碳酸氢根离子的电离生成氢氧化铝沉淀和碳酸根离子,则酸性:HCO3->Al(OH)3,故正确;
④N≡N键能大,性质稳定,则利用现象比较非金属性,事实为非金属性N>P,故错误;
⑤产生的气体能使湿润红色石蕊试纸变蓝,气体为氨气,则该晶体中一定有NH4+,故正确;
故选A.
②燃烧的镁条放入CO2中能继续燃烧,生成MgO和C,由还原剂的还原性大于还原产物的还原性可知,还原性为Mg>C,故正确;
③Na[Al(OH)4]溶液促进碳酸氢根离子的电离生成氢氧化铝沉淀和碳酸根离子,则酸性:HCO3->Al(OH)3,故正确;
④N≡N键能大,性质稳定,则利用现象比较非金属性,事实为非金属性N>P,故错误;
⑤产生的气体能使湿润红色石蕊试纸变蓝,气体为氨气,则该晶体中一定有NH4+,故正确;
故选A.
点评:本题考查化学实验方案的评价,为高频考点,涉及物质的性质、反应现象与结论的关系等,把握物质的性质及反应原理为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
 莽草酸是一种合成药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )| A、两种酸遇三氯化铁溶液都显色 |
| B、莽草酸分子和鞣酸分子中所含官能团相同 |
| C、等物质的量的两种酸与NaOH反应,消耗NaOH的量相同 |
| D、两种酸都能与溴水反应 |
下列有关实验装置进行的相应实验,不能达到实验目的是( )
A、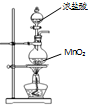 用装置制取氯气 |
B、 用装置除去氯气中的少量氯化氢和水蒸气 |
C、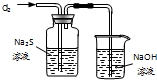 用装置可证明Cl2的氧化性强于S |
D、 用装置可以完成“喷泉”实验 |
 将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )
将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )| A、2.1mL | B、2.4mL |
| C、3.6mL | D、4mL |
 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.