题目内容
14.在短周期中X、Y可形成化合物XY3,下列叙述错误的是( )| A. | 若Y的原子序数为m,则X的原子序数可能为m+4 | |
| B. | XY3可能是离子化合物 | |
| C. | X、Y可能同周期,也可能同主族 | |
| D. | XY3可能是原子晶体 |
分析 根据短周期中的X和Y两种元素可组成化合物XY3,X、Y的化合价为+3、-1价时,可能分别在ⅢA、ⅤⅡA;X、Y的化合价为+6、-2价时可能均在ⅥA;还有可能为NH3,以此解答该题.
解答 解:根据短周期中的X和Y两种元素可组成化合物XY3,X、Y的化合价为+3、-1价时,可能分别在ⅢA、ⅤⅡA;X、Y的化合价为+6、-2价时可能均在ⅥA;还有可能为NH3,
A.如Y为H,则X可能为B等,B的原子序数比H大4,故A正确;
B.如为AlF3,则为离子化合物,故B正确;
C.如为SO3,则为同主族,如为AlCl3,则为同周期,故C正确;
D.由以上分析可知可能为AlF3、SO3或NH3或AlCl3等,不可能为原子晶体,故D错误.
故选D.
点评 本题考查学生利用元素在周期表中的位置来解答,熟悉常见的化合物是解答本题的关键,难度不大,注意利用化合价来分析元素在周期表中的位置即可解答.

练习册系列答案
相关题目
4.NA为阿伏伽德罗常数,下列说法正确的是( )
| A. | 1L0.1mol/L的NaF溶液中,含F-的数目小于0.1NA | |
| B. | 电解食盐水产生2gH2时转移的电子数为2NA | |
| C. | 标况下22.4L溴所含分子数目为2NA | |
| D. | 同温同压下,原子数均为NA的氢气和氦气具有相同的体积 |
5. 将CO2气体缓缓通入到含有等物质的量的KOH、Ba(OH)2和KAlO2的混合溶液中,直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示(假设每步反应均完全).下列关于整个反应进程中的各种描述不正确的是( )
将CO2气体缓缓通入到含有等物质的量的KOH、Ba(OH)2和KAlO2的混合溶液中,直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示(假设每步反应均完全).下列关于整个反应进程中的各种描述不正确的是( )
 将CO2气体缓缓通入到含有等物质的量的KOH、Ba(OH)2和KAlO2的混合溶液中,直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示(假设每步反应均完全).下列关于整个反应进程中的各种描述不正确的是( )
将CO2气体缓缓通入到含有等物质的量的KOH、Ba(OH)2和KAlO2的混合溶液中,直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示(假设每步反应均完全).下列关于整个反应进程中的各种描述不正确的是( )| A. | d~e段沉淀的减少是由碳酸钡固体的消失所致 | |
| B. | b~c段反应的离子方程式是:2A1O2-+3H2O+CO2=2A1(OH)3↓+CO32- | |
| C. | 0~a段反应的化学方程式是:Ba(OH)2+CO2=BaCO3↓+H2O | |
| D. | a~b段与c~d段所发生的反应相同 |
9.物质的熔沸点能用键能大小解释的是( )
| A. | H2O>H2S | B. | N2>O2 | C. | Na>K | D. | SiO2>CO2 |
19.如图表示在常温下CH3COOH溶液中加水时溶液的导电性变化,下列叙述不正确的是( )
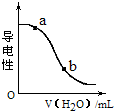

| A. | a点:c(H+)>c(CH3COO-)>c(OHˉ) | |
| B. | b点:c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 已知常温下,物质的量浓度相等的CH3COONa与CH3COOH混合液的pH<7,在此溶液中继续加CH3COONa至pH=7,则此时溶液中存在:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) | |
| D. | CH3COOH溶液的pH:a>b |
3.下列各组多电子原子的原子轨道能量高低比较中,错误的是( )
| A. | 3px<3py | B. | 2s<2p | C. | 3s<3d | D. | 4s>3p |
6.各组性质比较的表示中,正确的是( )
| A. | 生成由易到难:HF>HCl>HBr>HI | B. | 稳定性:HF<HCl<HBr<HI | ||
| C. | 酸性:HF>HCl>HBr>HI | D. | 酸性:HClO4<HBrO4<HIO4 |
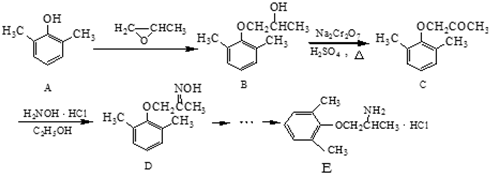
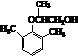 .
. .
.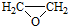 ).
).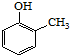 )和乙醇为原料制备
)和乙醇为原料制备 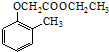 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用). ,食醋中的有机物结构式
,食醋中的有机物结构式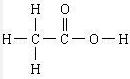 ,乙烯水化法所得产物的结构简式CH3CH2OH.
,乙烯水化法所得产物的结构简式CH3CH2OH.