题目内容
13.下列实验操作中,正确的是( )| A. | 用量筒量取10.00mL溶液 | B. | 用酒精萃取碘水中的碘 | ||
| C. | 用托盘天平称取2.50g固体 | D. | 用分液漏斗分离乙酸乙酯和水 |
分析 A.量筒精确度为0.1mL;
B.酒精与水混溶;
C.托盘天平精确度为0.1g;
D.分液漏斗可以将互不相溶的两层液体分开.
解答 解:A.量筒精确度为0.1mL,不能量取精确度为0.01mL的液体,故A错误;
B.萃取剂应不溶于水,酒精与水混溶,不能用作萃取剂,故B错误;
C.托盘天平精确度为0.1g,不能称量精确度为0.01g 的固体,故C错误;
D.乙酸乙酯和水是互不相溶的两层液体,可以用分液漏斗分离,故D正确;
故选:D.
点评 本题考查了常用计量仪器和基础实验知识,明确量筒、托盘天平的精确度,熟悉萃取、分液的原理是解题关键,题目难度不大.

练习册系列答案
相关题目
4.水的状态除了气、液和固态外,还有玻璃态.它是由液态水急速冷却到165K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )
| A. | 水由液态变为玻璃态,体积一定缩小 | |
| B. | 玻璃态水不可能加工为规则的外形 | |
| C. | 玻璃态水中水分子间的作用力与冰中不完全相同 | |
| D. | 玻璃态水是分子晶体 |
1.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列事实不能说明上述观点的是( )
| A. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| B. | 苯在50℃~60℃时发生硝化反应而甲苯在30℃时即可 | |
| C. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| D. | 乙烯能发生加成反应,乙烷不能发生加成反应 |
8.“生物质”是指由植物或动物生命体衍生得到的物质的总称.作为人类解决能源危机重要途径之一的“生物质能”,主要指用树木、庄稼、草类等植物直接或间接提供的能量.下列说法不正确的是( )
| A. | 生物质能源是可再生的能源 | |
| B. | 生物质能来源于太阳能 | |
| C. | 使用沼气作为能源是利用生物质能的一种方式 | |
| D. | 生物质能的缺点是严重污染环境 |
18.为除去二氧化硫气体中混有的少量水蒸气,可使气体通过洗气瓶,洗气瓶中应盛有( )
| A. | 硫酸铜溶液 | B. | 浓硫酸 | C. | 纯碱溶液 | D. | 碱石灰 |
5.下列各组澄清溶液中离子能大量共存,且加入(或滴入)X试剂后发生反应的离子方程式书写正确的是( )
| 选项 | 离子组 | X试剂 | 离子方程式 |
| A | K+、H+、SO42- | 少量Ba(OH)2 | Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| B | Fe2+、Cl-、H+ | 少量NaNO3 | 3Fe2++NO3-+4H+═NO↑+2H2O+3Fe3+ |
| C | Na+、Fe3+、NO3- | 过量KSCN | Fe3++3SCN-═Fe(SCN)3↓ |
| D | NH4+、H+、HCO3- | 过量NaOH | NH4++H++HCO3-+3OH-═NH3•H2O+2H2O+CO32- |
| A. | A | B. | B | C. | C | D. | D |
2.下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是( )
| A. | 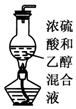 实验室制乙烯 | |
| B. | 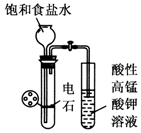 实验室制乙炔并验证乙炔能发生氧化反应 | |
| C. | 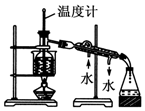 实验室中分馏石油 | |
| D. | 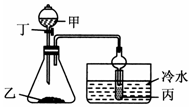 若甲为硫酸,乙为贝壳粉,丙为苯酚钠溶液,验证硫酸、碳酸、苯酚酸性的强弱 |
3.下列实验中不能观察到明显变化的是( )
| A. | 把溴水滴加到淀粉KI溶液中 | |
| B. | 把Cl2通入FeCl2溶液中 | |
| C. | 把绿豆大的钾投入少量水中 | |
| D. | 把一段打磨过的镁带放入少量冷水中 |