题目内容
下列属于强电解质的是( )
| A、H2S |
| B、CH3COONH4 |
| C、Cu |
| D、NH3?H2O |
考点:强电解质和弱电解质的概念
专题:
分析:强电解质是在水溶液中能完全电离的电解质,包括强酸、强碱、活泼金属氧化物和大部分盐.
解答:
解:A.硫化氢在水溶液中部分电离,属于弱电解质,故A错误;
B.醋酸铵是盐,在水溶液中能完全电离的电解质,属于强电解质,故B正确;
C.铜是单质,不是电解质,故C错误;
D.一水合氨在水溶液中部分电离,属于弱电解质,故D错误;
故选:B.
B.醋酸铵是盐,在水溶液中能完全电离的电解质,属于强电解质,故B正确;
C.铜是单质,不是电解质,故C错误;
D.一水合氨在水溶液中部分电离,属于弱电解质,故D错误;
故选:B.
点评:本题考查了强电解质的判断,难度不大,注意:电解质的强弱与电离程度有关,与溶液的导电能力无关,单质、混合物既不是电解质,又不是非电解质.

练习册系列答案
相关题目
常温下,下列各组离子能大量共存且有两种离子因对方的存在抑制了水解的是( )
| A、Na+、HCO3-、Cl-、SO42- |
| B、Al3+、K+、SO42-、Cl- |
| C、Fe2+、NH4+、SO42-、K+ |
| D、Mg2+、ClO-、OH-、HSO3- |
下列化学方程式或离子方程式中,书写正确的是( )
| A、氢氧化铜溶于醋酸溶液中:Cu(OH)2+2H+═Cu2++2H2O | |||
B、乙醛的银镜反应:CH3CHO+Ag(NH3)2OH
| |||
| C、苯酚钠溶液中通入少量二氧化碳:C6H5O-+CO2+H2O→C6H5OH+HCO3- | |||
D、丙烯聚合:nCH2=CHCH3
 |
在一容积为10L的密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4时刻测得A、B、C三种物质的物质的量如下表.据此判断下列结论中不正确的是( )
| 测定时刻/s | t1 | t2 | t3 | t4 |
| n(A)/mol | 7 | 3 | 1 | 1 |
| n(B)/mol | 5 | 3 | 2 | 2 |
| n(C)/mol | 1 | 3 | 4 | 4 |
| A、在容器中发生的反应为:2A+B?C |
| B、平衡时A的转化率比B的转化率高 |
| C、在该温度下该反应的化学平衡常数K=200 |
| D、在t1~t2内C物质的平均反应速率为[2/(t2-t1)]mol/(L?s) |
在一密闭烧瓶中,在25℃时存在如下平衡:2NO2(g)?N2O4(g)△H<0,将烧瓶置于100℃的水中,则下列几项性质中不会改变的是( )
①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度.
①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度.
| A、①和③ | B、③和⑤ |
| C、④和⑤ | D、②和④ |
下列有关化学反应能量变化的叙述一定正确的是( )
| A、生成物总能量大于反应物总能量,该反应为放热反应 |
| B、一个化学反应需要加热才能进行,该反应为吸热反应 |
| C、应用盖斯定律,可计算某些难以直接测量的化学反应焓变 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
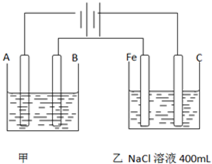 如图所示,外接电源为Zn-MnO2干电池,甲乙为相互串联的两个电解池,请回答:
如图所示,外接电源为Zn-MnO2干电池,甲乙为相互串联的两个电解池,请回答: