题目内容
10.将 4mol A 气体和 2mol B 气体在 2L 的密闭容器中混合并在一定条件下发生如下反应 2A(g)+B(g)?2C(g)△H<0. 4s后反应达到平衡状态,此时测得 C 的浓度为0.6mol•L-1.下列说法中正确的是( )| A. | 4 s(秒)时B的浓度为0.3 mol•L-1 | |
| B. | 4s内用物质A表示的反应速率为0.075 mol•L-1•s-1 | |
| C. | 达平衡后B的转化率为30% | |
| D. | 达平衡后若通入一定量氦气,A的转化率降低 |
分析 4s后反应达到平衡状态,此时测得 C 的浓度为0.6mol•L-1,生成C为0.6mol/L×2L=1.2mol,则
2A(g)+B(g)?2C(g)
开始 4 2 0
转化 1.2 0.6 1.2
平衡 2.8 1.4 1.2
A.结合c=$\frac{n}{V}$计算;
B.结合v=$\frac{△c}{△t}$计算;
C.结合转化率=$\frac{转化的量}{开始的量}$×100%计算;
D.2L 的密闭容器,达平衡后若通入一定量氦气,体系中各物质的浓度不变,平衡不移动.
解答 解:4s后反应达到平衡状态,此时测得 C 的浓度为0.6mol•L-1,生成C为0.6mol/L×2L=1.2mol,则
2A(g)+B(g)?2C(g)
开始 4 2 0
转化 1.2 0.6 1.2
平衡 2.8 1.4 1.2
A.4 s(秒)时B的浓度为$\frac{1.4mol}{2L}$=0.7mol•L-1,故A错误;
B.4s内用物质A表示的反应速率为$\frac{\frac{1.2mol}{2L}}{4s}$=0.015 mol•L-1•s-1,故B错误;
C.达平衡后B的转化率为$\frac{0.6mol}{2mol}$×100%=30%,故C正确;
D.2L 的密闭容器,达平衡后若通入一定量氦气,体系中各物质的浓度不变,平衡不移动,则A的转化率不变,故D错误;
故选C.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、速率及转化率的计算为解答的关键,侧重分析与计算能力的考查,注意选项D为解答的难点,题目难度不大.

 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案| A. | 水蒸气通过灼热的铁粉生成氢氧化铁和氢气 | |
| B. | Mg比Al活泼,更易与NaOH溶液反应生成H2 | |
| C. | Na在空气中长期放置最终变为Na2CO3粉末 | |
| D. | 向KClO3溶液中滴加AgNO3溶液得到白色AgCl沉淀 |
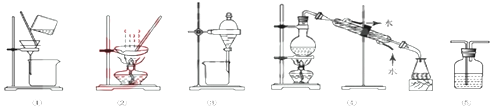
| A. | 分离Na2CO3溶液和CH3COOC2H5,选④ | B. | 粗盐提纯,选①和② | ||
| C. | 用FeC12溶液吸收C12,选⑤ | D. | 用CC14提取碘水中的碘,选③ |
| A. | 2nmol-1 | B. | $\frac{n}{m}$mol-1 | C. | $\frac{2n}{m}$mol-1 | D. | nmol-1 |
| A. | Cu与过量的S混合加热,最终得到CuS | |
| B. | AlCl3、FeCl2、FeCl3均可通过化合反应制得 | |
| C. | 常温下,将27 g A1投入足量18.4 mol•L-1的硫酸中,产生1.5 mol H2 | |
| D. | 将CO2不断通入Ca(OH)2溶液中,最终得到白色沉淀 |
| A. | 电池工作时锌为负极 | |
| B. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═2MnOOH+2OH- | |
| C. | 电池工作时,电解液的OH-移向正极 | |
| D. | 外电路中每通过0.2mol电子,锌的质量理论上减少6.5g |