题目内容
25℃时,相同物质的量浓度下列溶液中,水的电离度由大到小排列顺序正确的是( )
①KNO3 ②NaOH ③NH4Ac ④NH4Cl.
①KNO3 ②NaOH ③NH4Ac ④NH4Cl.
| A、①>②>③>④ |
| B、④>③>①>② |
| C、③>④>②>① |
| D、③>④>①>② |
考点:弱电解质在水溶液中的电离平衡,盐类水解的应用
专题:电离平衡与溶液的pH专题
分析:③CH3COONH4和④NH4Cl水解促进水的电离,①KNO3对水的电离无影响,②NaOH是强碱,抑制水的电离,以此解答该题.
解答:
解:③CH3COONH4和④NH4Cl水解促进水的电离,但③CH3COONH4发生互促水解,对水的电离促进更大;①KNO3对水的电离无影响;②NaOH是强碱,抑制水的电离,因此水的电离程度从大到小排列顺序正确的是③CH3COONH4④NH4Cl①KNO3②NaOH,
故选D.
故选D.
点评:本题考查水的电离平衡的影响因素,为高频考点,侧重学生的分析能力的考查,明确盐类的水解可促进水的电离、盐的电离使溶液呈酸性或碱性时抑制水的电离.

练习册系列答案
相关题目
对于0.1mol?L-1 Na2SO3溶液,正确的是( )
| A、升高温度,溶液的pH降低 |
| B、[Na+]=2[SO32-]+[HSO3-]+[H2SO3] |
| C、[Na+]+[H+]=2[SO32-]+2[HSO3-]+[OH-] |
| D、加入少量NaOH固体,[SO32-]与[Na+]均增大 |
关于炔烃的下列描述正确的是 ( )
| A、分子里含有碳碳三键的不饱和链烃叫炔烃 |
| B、炔烃分子里的所有原子都在同一直线上 |
| C、炔烃易发生加成反应,也易发生取代反应 |
| D、炔烃不能使溴水褪色,但可以使酸性高锰酸钾溶液褪色 |
下列烷烃的一氯取代物种没有同分异构体的是( )
| A、丙烷 | B、乙烷 |
| C、2-甲基丁烷 | D、3-甲基戊烷 |
在一个可以加热的密闭容器中,加入Na2O2和NaHCO3各0.5mol,将容器加热至400℃,待充分反应后排出气体,则容器中剩余的固体是( )
| A、Na2CO3 |
| B、Na2CO3和Na2O2 |
| C、NaOH |
| D、Na2CO3和NaOH |
燃烧等质量的下列烃,生成CO2最多的是( )
| A、CH4 |
| B、C6H6 |
| C、C2H6 |
| D、C3H6 |
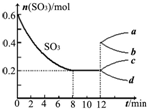 在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的变化如图所示:
在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的变化如图所示: