题目内容
如图图所示的装置中,有关说法不正确的是( )


| A、该装置实现化学能转变为电能 |
| B、该装置中Cu2+向Zn电极移动 |
| C、该装置外电路中电子由Zn棒转移到Cu棒 |
| D、该装置中Zn棒上的电极反应为:Zn-2e-═Zn2+ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:原电池是将化学能转变为电能的装置,Cu、Zn原电池中,Zn失去电子作负极,被氧化,正极上氢离子得到电子生成氢气,以此来解答.
解答:
解:A.该装置为原电池,可将化学能转化为电能,故A正确;
B.铜离子向正极移动,即向铜移动,故B错误;
C.电子由负极经外电路流向正极,即由锌流向铜,故C正确;
D.锌为负极,被氧化,电极方程式为Zn-2e-═Zn2+,故D正确.
故选B.
B.铜离子向正极移动,即向铜移动,故B错误;
C.电子由负极经外电路流向正极,即由锌流向铜,故C正确;
D.锌为负极,被氧化,电极方程式为Zn-2e-═Zn2+,故D正确.
故选B.
点评:本题考查原电池,为高频考点,侧重于学生的分析能力的考查,明确原电池中的能量转化及电极反应是解答本题的关键,注重基础知识的考查,题目较简单.

练习册系列答案
相关题目
福岛核电站泄漏的放射性物质中含有
I,下列有关
I的说法正确的是( )
131 53 |
131 53 |
A、
| ||
| B、由此可确定碘元素的相对原子质量为131 | ||
C、
| ||
D、
|
卤素单质具有相似的化学性质,这主要是由于卤素( )
| A、原子的最外层电子数相同,均为7个 |
| B、均为非金属元素 |
| C、单质均为双原子分子 |
| D、原子核外电子层数依次增大 |
下列化学用语对应正确的是( )
A、CH4分子的比例模型: |
B、CCl4的电子式: |
| C、H2O2的结构式:H-O-O-H |
| D、乙酸的最简式:C2H4O2 |
一定条件下,将1mol A和3mol B充入恒容容器中,发生如下反应:A(g)+3B(g)?2C(s),下列说法能说明该反应已经达到平衡状态的是( )
| A、气体的密度不再增大 |
| B、混合气体中A的体积分数不再变化 |
| C、混合气体的总压不再变化 |
| D、单位时间内生成a mol A,同时生成3a mol B |
化学与科学、技术、社会、环境、生活等密切相关.下列有关说法中错误的是( )
| A、液氨可用作制冷剂 |
| B、小苏打用于治疗胃酸过多 |
| C、明矾可用于自来水的杀菌消毒 |
| D、硅酸钠用于制备硅胶和木材防火剂的原料 |
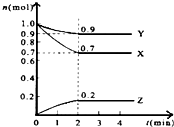 某实验小组对H2O2的分解做了如下探究:
某实验小组对H2O2的分解做了如下探究: